ソートリーダー
コードから治療へ: 次のAI革命には手と目が必要

エージェントシステム、XRスマートグラス、ロボティクスが人間を置き換えるのではなく、人間を支える
私たちは、人工知能におけるパラドックスを経験しています。
画面上では、AIは超人的です。大量の言語モデルは数秒で機能的なPythonコードを書きます。生成システムは数分で写真のようにリアルな画像や動画を生成します。ノーベル賞を受賞したシステムであるAlphaFoldは、既知のほぼすべてのタンパク質の構造を予測しました。デジタルでの勝利は積み重ねられています。
しかし、生物医学研究の物理的な世界では、発見のプロセスはまだ痛みを伴う手動での作業です。私たちは、AIが科学や医学を加速していることを感じていません。少なくとも今のところではありません。数字は問題の深さを明らかにしています。1500人以上の科学者を対象としたNatureの調査によると、70%以上の科学者が他の研究者の実験を再現しようとして失敗しています。さらに心配なことに、半分以上の科学者は自分の研究を再現できませんでした。がん生物学では、8年の再現性プロジェクトで、高影響の発見の40%のみが再現可能で、実験の68%には再現を試みるのに十分な文書化が欠けていました。
これは現代の科学の汚い秘密です。私たちには、発見の問題だけでなく、知識の取得の問題があります。重要な実験の詳細は、研究者の頭の中にあり、論文の中にはありません。プロトコルは変化します。暗黙の知識は、トレーニーが卒業すると出て行きます。出版された文献に基づいて訓練されたAIシステムは、これらのギャップをすべて継承します。
根本的な問題は、AIががん治療用の新しいタンパク質をデジタルシミュレーションで設計できるのに、試験するためのパイプを拾うことができないことです。汚い、予測不可能なウェットラボの現実をナビゲートして、自分の仮説を検証することができないのです。経験豊富な科学者の手を見て、実験をうまくいくようにするための繊細なテクニックを学ぶことができないのです。
この「実行ギャップ」は、AI革命が医療革命になることを妨げている最大のボトルネックです。ほとんどのロボティクス企業は、まだ機械に洗濯物を折ったり食器を積み込んだりすることを教えている間に、医学などの分野でのこれらの進歩の真正な変革的な能力に後れを取っています。
これを解決するには、チャットボットを超えて、AI共同研究者、つまりデジタルと物理の世界の橋渡しとなるエージェントシステムに向けて進む必要があります。スタンフォードでは、LabOSを開発しています。これは、AIエージェント、拡張現実(XR)スマートグラス、協調ロボティクスがどのようにしてこのループを閉じ、科学実験を人間と機械の間の共同対話に変え、現在失われている知識を自動的に取得するかを示しています。
大きな違い: AIに「目」と「手」が必要な理由
最も目立つAIの勝利は、環境が完全にデジタルである場所で起こりました: コードリポジトリ、キュレーションデータセット、またはシミュレートされたベンチマーク(ここでAIは仮想企業を実行したり、デジタルで株式に投資したりします)。
ウェットラボは異なります。生物学、そして一般的に科学的発見は、非常にノイジーなプロセスです。機器はドリフトし、オペレーターは即興で作業し、「プロトコル」はчастに人の頭の中にあります。クリーンな結果と失敗した実行の違いは、パイペッティングの角度、ボルテクシングパターン、試薬の置換、または10分長くインキュベーションが実行されたかどうかです。これらのコンテキストの詳細は、ほとんどの場合、論文には記載されません。ただし、AIモデルがデータセットを超えて一般化するには、これらの詳細が必要です。
そのため、ラボグレードのAIには、目(コンテキストで何が起こっているかを認識するため)、手(高分散ステップを標準化して安全に自動化するため)、メモリ(実際に何が起こったかを記録するため)が必要です。これらの機能がないと、モデルは勧告することはできますが、勧告を信頼性の高い物理的な実行に翻訳したり、計画が現実から乖離したときに失敗を説明したりすることはできません。
チャットボットを超えて: コパイロットからコサイエンティストへ
「エージェントAI」という用語は、ときどき緩く使用されます。生物医学的環境では、正確な意味で使用する必要があります: 目標(たとえば、「CRISPR遺伝子編集の効率を最適化し、オフターゲットを最小限に抑える」)をとり、タスクのシーケンスに分解し、ツールをまたいでタスクを実行し、結果を評価し、制約の下で監査可能な意思決定で計画を適応させることができるシステムです。
これは重要です。研究ワークフローは、単一のモデルコールではありません。仮説の生成、実験設計、データ処理、統計的テスト、解釈を含むエンドツーエンドのパイプラインです。最近の薬剤発見における思考は、ステップを単に加速するのではなく、これらのパイプラインをスケールするエージェントシステムを強調し始めています(たとえば、Unite.AIの小分子発見におけるエージェントについての議論)。
ソフトウェアエンジニアリングでは、AIコパイロットが開発者の生産性を高めることができる初期の経験的証拠をすでに見てきました。生物医学では、機会はコードを書くことだけではありません。プロトコルを書き、データを構造化し、実行を監視し、予測と測定のループを閉じ、AIをラボの人間の科学者に接続することです。
LabOS: AIが未来のラボのオペレーティングシステムで動くとき
スタンフォードでの私たちの仕事、遺伝子編集コパイロットのようなCRISPR-GPTやAI-XR共同実行システムのようなLabOSを開発しています。科学者が生物医学および材料科学のラボで協力して作業できるように、AIエージェント、拡張現実(XR)スマートグラス、協調ロボティクスがどのようにしてこのギャップを埋めるかを探っています。
1. デジタル(ドライ)ラボと物理(ウェット)ラボを結びつけるエンドツーエンドの「ラボオペレーティングシステム」を設計します。
前提は単純です。ラボノートブックが科学の記憶であるなら、ラボOSは実行レイヤーでなければなりません。意図をキャプチャし、それをアクションに翻訳し、結果を観察し、毎回実行を構造化された知識に変える必要があります。
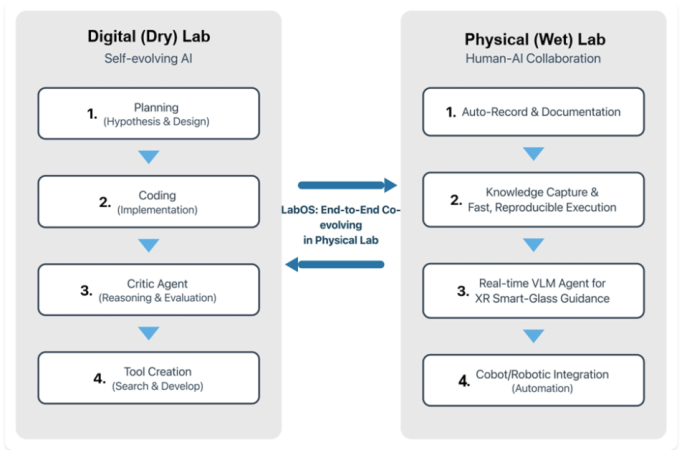
図。LabOSが自己進化するデジタルラボループ(計画、コーディング、批評、ツール作成)を人間とAIのウェットラボループ(自動ドキュメント、知識の取得、XRガイダンス、ロボティクスの統合)と結びつける概念的なビュー。
2. デジタルラボでのAI – 自己進化する計画とツールビルディング
デジタル(ドライ)ラボでは、AIにすでに得意なことをさせます。検索、統合、提案をさせます。しかし、自己改善もさせたいのです。新しい科学を「妄想」するのではなく、フィードバックからより良いツールやワークフローを学ぶことでです。
実用的デジタルラボループは、4つの反復ステージで構成できます。
- 計画(仮説 + 設計): 仮説を提案し、実験変数を選択し、混入変数を予測し、測定可能なエンドポイントを指定します。
- コーディング(実装): 分析スクリプト、シミュレーションパイプライン、適切な場合には機器制御テンプレートを生成または適応させます。
- 批評エージェント(推論 + 評価): 假定をストレステストし、統計的パワーをチェックし、コントロールを提案し、可能な失敗モードをフラグします。
- ツール作成(検索 + 開発): ワークフローにコンポーネント(パーサー、QCルーチン、ダッシュボード)が欠けている場合、ビルドしてツールキットに追加します。
3. 物理ラボでのAI – 「目」と「手」
物理(ウェット)ラボは、システムが信用を得るか、失うかを判断する場所です。目標は科学者を置き換えることではなく、摩擦とエラーを減らしながら観察可能性を高めることです。
私たちは物理ラボループを4つの補完的な機能と見なします。
- 自動記録と文書化: アクション、タイムスタンプ、機器の設定、逸脱を自動的にキャプチャし、文書化があとまわしになることを避けます。
- 再現可能な実行のための知識の取得: 実行を構造化された、クエリ可能なアーティファクト(プロトコルバージョン、パラメータセット、QCの結果)に変え、データ管理の原則(たとえばFAIR)に沿います。
- XRスマートグラスによるリアルタイムビジョン言語ガイダンス: マルチモーダルモデルを使用してシーン(オペレーターが何をしているか、どの試薬を持っているか)を解釈し、ステップバイステップのガイダンスとセーフティチェックを提供します。AR/XRは、実験のガイダンス(Stanford、Princeton、NVIDIAとの共同研究)のような高リスクの物理ワークフローで価値を実証しています。
- コボット/ロボティクスの統合による自動化: 繰り返しのステップを標準化し、安全なハンドオーバーを可能にし、変動を減らします。シミュレーションからリアルワールドへのワークフロー(たとえばNVIDIA Isaac)や、LabOSのスマートグラスのライブストリーミングと人間とAIのインタラクションのようなエッジでのリアルタイムAI処理は、重要なエナブルリングレイヤーです。
このアーキテクチャは、分野全体のより広い方向性と一致しています。つまり、「セルフドライブ」または「オートノマスラボラトリー」は、実験の次のステップを計画するために、自動化と機械学習を組み合わせることです。LabOSが追加するのは、透明性を犠牲にせずに、人間のインターフェイスレイヤーを緊密に結合することです。
LabグレードのAIは「データセット上のAI」だけではない
生物医学/科学的スーパーアイのためのAIシステムは、過去の評価または試験で印象的なものですが、物理ラボでは実行時に期待を裏切ることがあります。理由は、単一のバグではありません。通常は、モデルの仮定とラボの現実との間のミスマッチです。
3つのギャップが繰り返し現れます。
- コンテキストギャップ: データセットは、オペレーターが重要であると考えているコンテキスト変数(温度の逸脱、試薬のロット番号、プロトコルの微妙な逸脱)を通常省略しています。
- アクションギャップ: 多くのAIシステムは、何をしなければならないかを勧告できますが、勧告を信頼性の高い物理的なステップに翻訳することはできません。
- フィードバックギャップ: 実行からの構造化された、高品質のフィードバックがなければ、モデルはどこで失敗するかを学ぶことができません。科学者は、なぜ失敗したのかを監査することもできません。
これらのギャップを閉じることは、新しいニューラルネットワークアーキテクチャを発明することではなく、ラボを機械に読み取れるようにするためのインストルメンテーション、インターフェイス、データ契約を構築することです。AIが人間と一緒に作業できるようにします。
デザインによる信頼: アクション可能なAIのためのセーフティとガバナンス
発見研究におけるエージェントAIは、精度に関する既存の懸念だけではなく、新しい失敗モードを引き起こします。なぜなら、AIはアクションを起こすことができるからです。ラボでは、アクションは、廃棄物、損害、または誤解を招く結論の可能性を意味します。特に、実験が臨床的仮説にフィードする場合にそうです。
役立つ心構えは、AIを使用したラボスタックを、保証が必要なソシオテクニカルシステムとして扱うことです。いくつかの既存のフレームワークが役立ちますが、ラボの現実に翻訳される必要があります。
- リスクマネジメントを継続的な実践として: NISTのAIリスクマネジメントフレームワーク(AI RMF 1.0)は、AIリスクをライフサイクル全体でマッピング、測定、管理するための実用的ボキャブラリーを提供します。
- 医療関連AIのための規制への準拠: FDAのAI/MLソフトウェアとしての医療機器(SaMD)の取り組み、アクションプランと関連ガイドラインを含む、は、患者ケアに影響を与えるAIの「良い実践」の具体的なビューを提供します。
遺伝子編集などの高影響ドメインについては、すでに世界的な議論が行われています。人ゲノム編集について、適切な監視メカニズムと責任あるガバナンスの必要性を強調する推奨事項が議論されています。たとえば、アメリカ遺伝子・細胞治療学会(ASGCT)による推奨事項があります。LabOSのようなシステムは、コンプライアンスをより簡単にし、より困難にすべきではありません。
チェックリスト: 科学的発見のための安全なAI共同研究者のコントロール
私たちの見解では、安全性に配慮したラボOSは、少なくとも次のデザインを実装する必要があります。
- デフォルトのプロバンス: すべてのデータセット、プロトコルバージョン、モデル出力は、入力とタイムスタンプに追跡可能である必要があります。
- バウンダードオートノミー: システムには、明示的な許可(確認なしで実行できること)とエスカレーションルール(確認を求める必要があるとき)が必要です。
- 人間のオーバーライドとグラシアスディグレーション: センサーまたはデータストリームが故障した場合、または不確実性が高い場合、システムはより安全で、より単純なモードにフォールバックする必要があります。
- 継続的な検証: シミュレーションによる予測は、物理ラボでの検証とペアにする必要があります。物理ラボでの実行には、AIモデル/エージェントに戻って結論を伝える前に、QCゲートを含める必要があります。
- セキュリティと二次使用の認識: ラボインフラストラクチャを改ざんから保護します。
人間をどこにでもエンパワーする: AI共同研究者はプレイヤーを均等にすることができますか?
AI-XR「共同研究者」の最も魅力的な約束の1つは、エリート機関へのスピードだけではありません。誰にでもアクセス性を提供することです。現在、どのようなものが小さなラボ、スタートアップ、リモート/農村/地域クリニックを制限しているかを考えてみましょう。
- 専門家の専門知識へのアクセスが限られている(ゴールドスタンダードプロトコルと機器)。
- トレーニング、ミス、再作業の相対コストが高い。
- ツールが断片化しています。ノートブック、スプレッドシート、機器ログ、分析スクリプトは、ほとんどの場合、クリーンに接続されていません。
コンテキストで実行をガイドする(XRグラスを介して)、自動的に何が起こったかをキャプチャし、先に進むための次のベストステップを提案することができるシステムは、高度なアッセイをサイト間で再現可能にすることができます。原則として、プロトコルが一貫して実行される必要がある分散型臨床研究をサポートすることもできます。
タイムライン: どの科学者や臨床医もコサイエンティストを得ることができるのはいつですか?
簡単に言えば、タスク(たとえば、ラボで信頼性の高い薬剤を生成すること)については、多くの場合、より近い将来(1年以内)ですが、他のタスク(たとえば、AIが完全にがんやアルツハイマー病を解決すること)については、デモが示唆するよりも遠い将来(3年以上)です。現実的なロードマップは次のとおりです。
- 近い将来(1年以内): ワークフローのコパイロットが管理負担を軽減します。プロトコル草案、文献の統合、分析テンプレート、自動QCレポート。制限要因は統合であり、モデル能力ではありません。
- 中期(1〜2年): ラボでの共同実行システム。XRグラスガイダンス、自動文書化、繰り返しのステップのロボティクス。信頼性は監査トレイルとタイトな人間のループデザインに依存します。
- 長期(3年以上): 発見と翻訳を接続するドメイン間の共同研究者。ラボデータを臨床的エンドポイントに接続し、セーフティシグナルを監視し、試験を設計することを支援します。規制と倫理的期待に従っています。
コードから治療へ: 1000倍の科学的発見への道
LabOSは、実験が人間と機械の間の対話として実行できるかどうかを問う単純な質問に答える試みです。実行、証拠、意図がエンドツーエンドで接続されます。システムをうまく構築すれば、生物医学や物理科学の多くの分野で発見の遅れを引き起こすギャップに取り組むことができます。構築がうまくいかない場合は、非再現性を増幅させ、新しい安全性のリスクを生み出します。
次の数年間で最も重要な作業は基盤的なものです。標準化されたデータとデバイスインターフェイスの構築(オペレーティングシステムを構築すること、多くの種類のアプリを実行するiOSのように)、LabOSのLabSuperVisionベンチマークのような実行と不確実性を含むAIベンチマークの構築、そして、革新を促進しながら患者と研究の完全性を保護する実世界への展開の開始です。
研究者や臨床医にとって、質問は、AIがラボに入ってくるかどうかではありません。すでに入ってきています。質問は、ツールのコレクションとして統合するか、信頼性の高いシステムとして設計されたものか、生物医学科学の現実に合わせて設計されたものかです。
推奨文献およびソース
- 再現性調査(Nature、2016): https://www.nature.com/articles/533452a
- CRISPR-GPTの同行審査付き論文(Nature Biomedical Engineering): https://www.nature.com/articles/s41551-025-01463-z
- スタンフォードメディシンのニュース: AIとCRISPR遺伝子編集(2025): https://med.stanford.edu/news/all-news/2025/09/ai-crispr-gene-therapy.html
- LabOSのプレプリント(arXiv): https://arxiv.org/abs/2510.14861
- LabOSとLabSuperVisionベンチマークのウェブサイト: https://ai4lab.stanford.edu
- NIST AIリスクマネジメントフレームワーク(AI RMF 1.0): https://nvlpubs.nist.gov/nistpubs/ai/NIST.AI.100-1.pdf
- FDAのAI/MLソフトウェアとしての医療機器の概要: https://www.fda.gov/medical-devices/software-medical-device-samd/artificial-intelligence-software-medical-device
- FAIRデータ原則(Scientific Data、2016): https://doi.org/10.1038/sdata.2016.18
- Unite.AIによる小分子薬剤発見のボトルネック: https://www.unite.ai/how-ai-is-breaking-down-the-bottlenecks-in-small-molecule-drug-discovery/
- Unite.AIによるAIとロボット外科手術: https://www.unite.ai/how-ai-is-ushering-in-a-new-era-of-robotic-surgery/












