Hälso- och sjukvård
Google DeepMind presenterar AlphaGenome för att avkoda den mänskliga genomens funktion
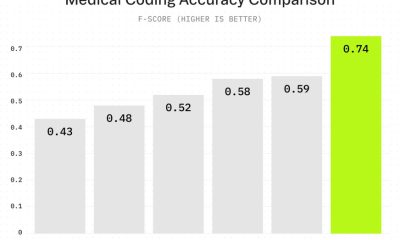
Google DeepMind släppte AlphaGenome den 28 januari, en AI-modell som förutsäger hur DNA-sekvenser översätts till biologiska funktioner, bearbetar upp till en miljon baspar samtidigt och presterar bättre än befintliga modeller i 25 av 26 varianteffektprediktionsbenchmark.
Modellen, publicerad i Nature och detaljerad på DeepMind-bloggen, representerar ett betydande framsteg inom beräkningsgenomik. Där tidigare modeller krävde separata system för olika prediktionsuppgifter hanterar AlphaGenome allt från genuttryck till kromatintillgänglighet i en enda enhetlig arkitektur.
“AlphaGenome kan titta på en lång sträcka av DNA och förutsäga var de kritiska reglerande elementen är och deras nedströms effekter på genuttryck”, skrev DeepMind-teamet i sitt tillkännagivande. Modellens miljontokenkontextfönster tillåter den att fånga långdistansinteraktioner mellan avlägsna DNA-regioner som påverkar hur gener slås på och av.
Hur det fungerar
AlphaGenome kombinerar två neurala nätverksarkitekturer: en Borzoi-liknande 1D-convolutionsnätverk för bearbetning av råa DNA-sekvenser och en U-Net-arkitektur anpassad från bildsegmentering. Denna hybrida approach låter modellen hantera både den sekventiella naturen hos DNA och de komplexa rumsliga relationerna mellan reglerande element.
Träningsdata omfattar ungefär 7 000 genomska spår från ENCODE- och FANTOM-konsortierna – massiva samarbetsinsatser som har katalogiserat funktionella element över hela den mänskliga genomen. Modellen lär sig att förutsäga signaler från experimentella tester som mäter genuttryck, DNA-tillgänglighet, proteinbindning och kromatinförändringar.
För forskare ligger den praktiska värdet i varianteffektprediktion. När en patients genom innehåller en mutation behöver kliniker veta om den varianten har betydelse. AlphaGenome kan förutsäga hur en enda nukleotidändring påverkar hela reglerande landskapet, möjligtvis flaggande sjukdomsorsakande varianter som nuvarande metoder missar.
Modellen uppnådde starka resultat på benchmark-tester som testade dess förmåga att förutsäga hur genetiska varianter påverkar genuttryck och reglerande elementaktivitet. För uttrycksquantitativa locus (eQTL) – varianter som är kända för att påverka genuttrycksnivåer – matchade eller överträffade AlphaGenome specialiserade modeller som tränats specifikt för dessa uppgifter.
Öppen källkods tillgänglighet
DeepMind släppte AlphaGenomes källkod på GitHub för icke-kommersiellt bruk, fortsätter labbets mönster att göra grundläggande biologiverktyg allmänt tillgängliga. Lagret innehåller modellvikter, inferenskod och dokumentation för att köra förutsägelser på anpassade sekvenser.
Den öppna utgåvan följer modellen etablerad av AlphaFold, DeepMinds proteinstrukturprediktionsverktyg som har använts av över 3 miljoner forskare sedan dess utgåva 2021. AlphaGenome hanterar ett kompletterande problem: medan AlphaFold förutsäger hur proteiner ser ut, förutsäger AlphaGenome när och var gener producerar dessa proteiner.
Google DeepMind VD Demis Hassabis har positionerat biologi som en primär tillämpningsdomän för labbets AI-förmågor. Genomarbetet utvidgar DeepMinds ambitioner bortom konversations-AI och språkmodeller som driver produkter som Gemini, tillämpar liknande arkitektoniska innovationer på vetenskapliga problem.
Varför detta är viktigt
Den mänskliga genomen innehåller ungefär 3 miljarder baspar, men endast cirka 1,5% kodar direkt för proteiner. Den återstående 98,5% – tidigare avfärdad som “skräp-DNA” – innehåller reglerande element som kontrollerar när, var och hur mycket gener uttrycks. Mutationer i dessa icke-kodande regioner orsakar sjukdomar, men att identifiera vilka varianter som har betydelse har varit oerhört svårt.
Traditionella metoder kräver dyra, tidskrävande experiment för att testa enskilda varianter. Maskinlärningsmodeller som AlphaGenome kan skärma tusentals varianter beräkningsmässigt, prioritera vilka som förtjänar experimentell uppföljning. För sällsynta sjukdomsdiagnoser, där patienter ofta bär nya varianter med okända effekter, kan denna funktion accelerera vägen från sekvensering till diagnos.
Modellens förmåga att bearbeta miljontals basparkontexter är särskilt betydelsefull. Genreglerande element kan sitta hundratusentals baspar bort från de gener de kontrollerar, kommunicerar genom komplex 3D-vikning av DNA. Tidigare modeller med kortare kontextfönster kunde inte fånga dessa långdistansberoenden.
AlphaGenome ansluter sig till en växande ekosystem av AI-verktyg som omvandlar biologisk forskning. Proteinstrukturprediktion, läkemedelsupptäckt och nu genreglering är alltmer hanterbara problem för maskinlärning. För genetisk forskningssamhälle demokratiserar den öppna tillgängligheten av dessa modeller tillgången till beräkningsförmågor som tidigare var begränsade till välfinansierade laboratorier.
Modellens begränsningar är också tydliga från DeepMinds presentation. Medan AlphaGenome excellerar vid att förutsäga experimentella mätningar, kräver översättningen av dessa förutsägelser till kliniska resultat ytterligare validering. Gapet mellan att förutsäga kromatintillgänglighet och förutsäga sjukdomsrisk förblir betydande.
För nuvarande fungerar AlphaGenome som ett forskningsverktyg – ett som kan accelerera förståelsen av hur genomen fungerar, även om kliniska tillämpningar förblir år bort. De 3 000 forskare i 160 länder som redan använder modellen tyder på att forskarsamhället ser omedelbar värde i vad DeepMind har byggt.