विचार नेता
कोड से इलाज तक: अगली एआई क्रांति को एक हाथ (और आंखें) की आवश्यकता है

कैसे एजेंटिक सिस्टम, एक्सआर स्मार्ट ग्लास, और रोबोटिक्स मानवों को सशक्त बनाएंगे – उन्हें प्रतिस्थापित नहीं करेंगे
हम एक विरोधाभास के माध्यम से जी रहे हैं जो कृत्रिम बुद्धिमत्ता में है।
स्क्रीन पर, एआई सुपरमैन है। बड़े भाषा मॉडल कुछ सेकंड में कार्यात्मक पाइथन कोड लिखते हैं। उत्पन्न प्रणाली मिनटों में फोटोरियलिस्टिक छवियों और वीडियो का उत्पादन करती है। नोबेल पुरस्कार विजेता प्रणाली जैसे अल्फाफोल्ड ने लगभग सभी ज्ञात प्रोटीन की संरचना की भविष्यवाणी की है। डिजिटल जीत ढेर हो रही है।
हालांकि, जैव चिकित्सा अनुसंधान की भौतिक दुनिया में, खोज की प्रक्रिया अभी भी दर्दनाक रूप से मैनुअल है। हम वास्तव में एआई को विज्ञान या चिकित्सा में तेजी लाने की अनुभूति नहीं कर रहे हैं, कम से कम अभी तक नहीं। संख्या समस्या की गहराई को उजागर करती है। 1,500 से अधिक वैज्ञानिकों के एक नेचर सर्वेक्षण में पाया गया कि 70% से अधिक ने किसी अन्य शोधकर्ता के प्रयोगों को दोहराने की कोशिश की और विफल रहे। और भी परेशान करने वाली बात: अधिकांश अपने स्वयं के काम को दोहरा नहीं सकते थे। कैंसर जीव विज्ञान में विशेष रूप से, एक आठ साल की पुनरुत्पादकता परियोजना में पाया गया कि केवल 40% उच्च प्रभाव वाले निष्कर्षों को दोहराया जा सकता था और 68% प्रयोगों में प्रतिलिपि करने के लिए पर्याप्त दस्तावेज़ीकरण की कमी थी।
यह आधुनिक विज्ञान का गंदा रहस्य है: हमारे पास एक ज्ञान अधिग्रहण समस्या है, न कि केवल एक खोज समस्या। महत्वपूर्ण प्रायोगिक विवरण शोधकर्ताओं के सिर में रहते हैं, कागजात में नहीं। प्रोटोकॉल ड्रिफ्ट होते हैं। सूक्ष्म ज्ञान तब निकल जाता है जब प्रशिक्षुओं को स्नातक की उपाधि मिलती है। एआई सिस्टम प्रकाशित साहित्य पर प्रशिक्षित होते हैं जो इन सभी अंतराल को विरासत में मिलता है।
मूल समस्या यह है कि जबकि एक एआई कैंसर चिकित्सा के लिए एक नए प्रोटीन को डिजिटल सिम्युलेशन में डिजाइन कर सकता है, यह एक पिपेट उठाने के लिए नहीं सकता है यह परीक्षण करने के लिए। यह एक गीले प्रयोगशाला की गंदी, अप्रत्याशित वास्तविकता को नेविगेट नहीं कर सकता है ताकि यह अपनी खुद की परिकल्पना को मान्य कर सके। यह एक अनुभवी वैज्ञानिक के हाथों को देख नहीं सकता है और उन सूक्ष्म तकनीकों को सीख नहीं सकता है जो प्रयोगों को काम करते हैं।
यह “निष्पादन अंतर” एआई क्रांति को एक चिकित्सा क्रांति में बदलने से रोकने वाली सबसे बड़ी बोतलनेक है। जबकि अधिकांश रोबोटिक्स कंपनियां अभी भी मशीनों को कपड़े धोने या डिशवॉशर लोड करने की शिक्षा देने में व्यस्त हैं, वे चिकित्सा जैसे क्षेत्रों में इन प्रगति की वास्तव में परिवर्तनकारी क्षमताओं से पीछे हैं।
इसे हल करने के लिए, हमें चैटबॉट्स से परे जाना होगा और एआई सह-वैज्ञानिकों की ओर बढ़ना होगा, एजेंटिक सिस्टम जो डिजिटल और भौतिक दुनिया के बीच की खाई को पुल करते हैं, योजना और कोडिंग से परे और वास्तविक दुनिया के निष्पादन में आगे बढ़ रहे हैं। स्टैनफोर्ड में, हम LabOS विकसित कर रहे हैं, एक डिजिटल-भौतिक एआई ढांचा जो प्रदर्शित करता है कि एआई एजेंट, एक्सटेंडेड रियलिटी (एक्सआर) स्मार्ट ग्लास, और सहयोगी रोबोटिक्स कैसे मिलकर इस लूप को बंद कर सकते हैं, वैज्ञानिक प्रयोगों को मानव और मशीन के बीच एक सहयोगी बातचीत में बदल देते हैं, जबकि स्वचालित रूप से ज्ञान को पकड़ते हैं जो वर्तमान में खो जाता है।
महान विभाजन: क्यों एआई को “आंखें” और “हाथ” की आवश्यकता है
एआई की सबसे दिखाई देने वाली जीत में से कई ऐसे क्षेत्रों में हुई हैं जहां वातावरण पूरी तरह से डिजिटल है: कोड रिपॉजिटरी, क्यूरेटेड डेटासेट, या सिम्युलेटेड बेंचमार्क (जहां एआई एक आभासी व्यवसाय चलाने या डिजिटल रूप से स्टॉक में निवेश करने के लिए प्रतिस्पर्धा करता है)।
गीली प्रयोगशालाएं अलग हैं। जीव विज्ञान, और सामान्य रूप से वैज्ञानिक खोज, एक बहुत ही शोर प्रक्रिया है। उपकरण ड्रिफ्ट होते हैं, ऑपरेटर सुधार करते हैं, और “प्रोटोकॉल” अक्सर आंशिक रूप से लोगों के सिर में रहता है। एक साफ परिणाम और एक विफल रन के बीच का अंतर एक पिपेटिंग कोण, एक वोर्टेक्स पैटर्न, एक रीagent प्रतिस्थापन, या एक इनक्यूबेशन हो सकता है जो 10 मिनट लंबा चला गया। ये संदर्भ विवरण शायद ही कभी एक कागज में बनते हैं और वे ठीक वही हैं जो एक एआई मॉडल को डेटासेट से परे सामान्य करने के लिए चाहिए।
इसलिए लैब-ग्रेड एआई को आंखों (जो संदर्भ में हो रहा है उसे देखने के लिए) की आवश्यकता है, हाथ (उच्च-वेरिएंस चरणों को मानकीकृत और सुरक्षित रूप से स्वचालित करने के लिए), और स्मृति (वास्तव में क्या हुआ था उसे रिकॉर्ड करने के लिए)। इन क्षमताओं के बिना, मॉडल यह सिफारिश कर सकते हैं कि क्या करना है, लेकिन वे विश्वसनीय रूप से सिफारिशों को मान्य भौतिक निष्पादन में अनुवाद नहीं कर सकते हैं या विफलता की व्याख्या नहीं कर सकते हैं जब वास्तविकता योजना से विचलित होती है।
चैटबॉट्स से परे: कोपायलट से सह-वैज्ञानिक तक
एजेंटिक एआई शब्द का कभी-कभी ढीला उपयोग किया जाता है। जैव चिकित्सा सेटिंग्स में, यह कुछ सटीक मतलब होना चाहिए: एक प्रणाली जो एक लक्ष्य ले सकती है (उदाहरण के लिए, “सीआरआईएसपीआर जीन संपादन की दक्षता को अनुकूलित करें जबकि ऑफ-टार्गेट को कम करें”) और इसे कार्यों की एक श्रृंखला में तोड़ दें, उपकरणों के पार कार्यों को निष्पादित करें, परिणामों का मूल्यांकन करें, और सीमाओं के तहत योजना को अनुकूलित करें और लेखा परीक्षित निर्णय लेने के साथ।
यह महत्वपूर्ण है क्योंकि अनुसंधान कार्य प्रवाह एकल मॉडल कॉल नहीं हैं। वे हाइपोथेसिस फॉर्मूलेशन, प्रयोगात्मक डिजाइन, डेटा प्रोसेसिंग, सांख्यिकीय परीक्षण, और व्याख्या को शामिल करने वाली एंड-टू-एंड पाइपलाइनें हैं। हाल के विचारों में ड्रग डिस्कवरी ने एजेंटिक सिस्टम पर जोर देना शुरू किया है जो कि इन पाइपलाइनों को स्केल कर सकते हैं, न कि केवल व्यक्तिगत चरणों (जैसे Unite.AI के एजेंटों की चर्चा छोटे अणु ड्रग डिस्कवरी में) को तेज करते हैं।
सॉफ्टवेयर इंजीनियरिंग में, हमने पहले से ही एआई कोपायलट्स के लिए प्रारंभिक अनुभवजन्य प्रमाण देखा है जो डेवलपर थ्रूपुट बढ़ा सकते हैं। जैव चिकित्सा में, समान अवसर न केवल कोड लिखना है, बल्कि प्रोटोकॉल और डेटा को मान्य करना, निष्पादन की निगरानी करना, और भविष्यवाणी और माप के बीच लूप को बंद करना है, एआई को प्रयोगशालाओं में मानव वैज्ञानिकों से जोड़ना है।
LabOS: जब एआई लैब के लिए एक ऑपरेटिंग सिस्टम पर चलता है
स्टैनफोर्ड में हमारे काम में, एआई 4 साइंस पर, जीन-एडिटिंग कोपायलट्स जैसे सीआरआईएसपीआर-जीपीटी और एआई-एक्सआर सह-कार्यान्वयन प्रणाली जैसे लैबओएस जो जैव चिकित्सा और सामग्री विज्ञान प्रयोगशालाओं में वैज्ञानिकों की मदद करते हैं, हम एक स्थापत्य परिवर्तन का अन्वेषण कर रहे हैं:
1. एक अंत से अंत “लैब ऑपरेटिंग सिस्टम” का डिजाइन करना जो एक डिजिटल (सूखी) प्रयोगशाला को एक भौतिक (गीली) प्रयोगशाला से जोड़ता है।
पूर्वनिर्धारित यह है: यदि एक प्रयोगशाला नोटबुक विज्ञान की स्मृति है, तो एक लैब ओएस निष्पादन परत होनी चाहिए, जो इरादे को पकड़ती है, इसे क्रियाओं में अनुवाद करती है, परिणामों का अवलोकन करती है, और हर रन को संरचित ज्ञान में बदल देती है।
[कैप्शन id = “अटैचमेंट_421125” align = “aligncenter” width = “987”] 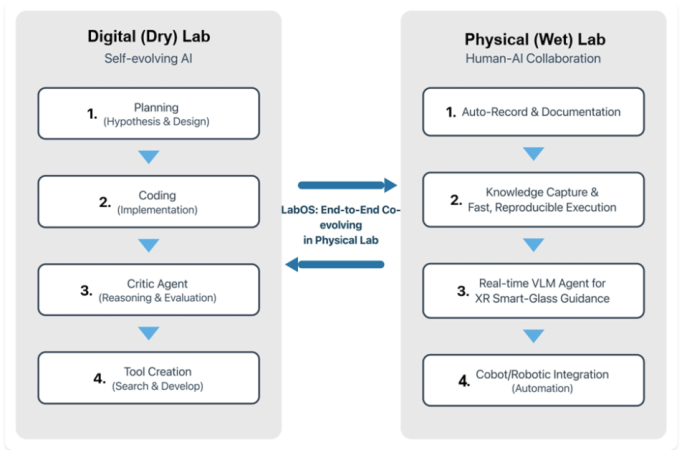
2. डिजिटल लैब में एआई – स्व-विकसित योजना और टूल-बिल्डिंग
डिजिटल (सूखी) प्रयोगशाला में, हम एआई को वही करने दे सकते हैं जो यह पहले से ही अच्छा करता है: खोज, संश्लेषण, और प्रस्ताव। लेकिन हम यह भी चाहते हैं कि यह स्व-सुधार हो। न कि “नई विज्ञान की कल्पना” द्वारा, बल्कि प्रतिक्रिया से बेहतर उपकरण और कार्य प्रवाह सीखने से।
एक व्यावहारिक डिजिटल-लैब लूप को चार बार-बार होने वाले चरणों के रूप में फ्रेम किया जा सकता है:
- योजना (हाइपोथेसिस + डिजाइन): हाइपोथेसिस का प्रस्ताव, प्रयोगात्मक चर का चयन, अप्रत्याशित कारकों की आशंका, और मात्रात्मक अंत बिंदुओं को निर्दिष्ट करें।
- कोडिंग (कार्यान्वयन): विश्लेषण स्क्रिप्ट, सिम्युलेशन पाइपलाइन, और उपकरण नियंत्रण टेम्पलेट्स उत्पन्न या अनुकूलित करें जहां उपयुक्त हो।
- आलोचना एजेंट (कारण + मूल्यांकन): धारणाओं को तनाव दें, सांख्यिकीय शक्ति की जांच करें, नियंत्रण का प्रस्ताव करें, और संभावित विफलता मोड को झंडा दें।
- टूल निर्माण (खोज + विकास): जब कार्य प्रवाह में एक घटक (एक पार्सर, एक क्यूसी दिनचर्या, एक डैशबोर्ड) की कमी होती है, तो इसे बनाएं और इसे टूलकिट में वापस जोड़ें।
3. भौतिक लैब में एआई – एआई के साथ “आंखें” (एक्सआर ग्लास) और “हाथ” (रोबोटिक्स)
भौतिक (गीली) प्रयोगशाला वह जगह है जहां सिस्टम या तो विश्वास अर्जित करता है – या इसे खो देता है। लक्ष्य वैज्ञानिक को प्रतिस्थापित नहीं करना है, बल्कि घर्षण और त्रुटि को कम करना है जबकि अवलोकनीयता बढ़ाना है।
हम भौतिक-लैब लूप को चार पूरक क्षमताओं के रूप में देखते हैं:
- स्वचालित रिकॉर्ड और प्रलेखन: क्रियाओं, टाइमस्टैम्प, उपकरण सेटिंग्स, और विचलन को स्वचालित रूप से कैप्चर करें, ताकि प्रलेखन एक बाद की बात न हो।
- ज्ञान अधिग्रहण तेजी से और पुनरुत्पादक निष्पादन के लिए: रन को संरचित, प्रश्नीय वस्तुओं (प्रोटोकॉल संस्करण, पैरामीटर सेट, क्यूसी परिणाम) में परिवर्तित करें जो डेटा स्टीवर्डशिप के सिद्धांतों जैसे फेयर के साथ संरेखित हैं।
- वास्तविक समय दृष्टि-भाषा मार्गदर्शन एक्सआर स्मार्ट ग्लास के माध्यम से: बहुमोड़ल मॉडल का उपयोग करके दृश्य की व्याख्या करें (जो ऑपरेटर कर रहा है, कौन सा रीagent हाथ में है) और चरण-दर-चरण मार्गदर्शन और सुरक्षा जांच प्रदान करें। एआर / एक्सआर ने पहले से ही उच्च-दांव वाले भौतिक कार्य प्रवाह में मूल्य का प्रदर्शन किया है, जैसे प्रयोगात्मक मार्गदर्शन (लैबओएस, स्टैनफोर्ड, प्रिंसटन, एनवीडिया के साथ सहयोग में)।
- कोबोट / रोबोटिक एकीकरण स्वचालन के लिए: पुनरावृत्ति चरणों को मानकीकृत करें, सुरक्षित हैंडओवर को सक्षम करें, और परिवर्तनशीलता को कम करें। सिम्युलेशन-टू-रियल कार्य प्रवाह (जैसे एनवीडिया आइजैक) और रियल-टाइम एआई प्रोसेसिंग जैसे स्मार्ट ग्लास लाइव स्ट्रीमिंग और मानव-एआई इंटरैक्शन में लैबओएस के लिए एज प्लेटफ़ॉर्म महत्वपूर्ण हैं।
यह वास्तुकला क्षेत्र में एक व्यापक दिशा के साथ संरेखित है: “स्व-ड्राइविंग” या स्वायत्त प्रयोगशालाएं जो योजना के अगले प्रयोग को जोड़ने के लिए स्वचालन के साथ मशीन लर्निंग को जोड़ती हैं। लैबओएस जो जोड़ता है वह एक तंग मानव इंटरफ़ेस परत है, ताकि स्वायत्तता पारदर्शिता की लागत पर न आए।
लैब-ग्रेड एआई क्यों “एआई ऑन ए डेटासेट” नहीं है
जैव चिकित्सा / वैज्ञानिक सुपर इंटेलिजेंस के लिए एआई सिस्टम अक्सर प्रतिगामी मूल्यांकन में प्रभावशाली दिखते हैं और परीक्षा में उत्तीर्ण होते हैं, और फिर भौतिक प्रयोगशाला में कम प्रदर्शन करते हैं। कारण अक्सर एकल बग नहीं है। यह आमतौर पर मॉडल की धारणाओं और प्रयोगशाला की वास्तविकता के बीच एक मismatch है।
तीन अंतर बार-बार दिखाई देते हैं:
- संदर्भ अंतर: डेटासेट आमतौर पर संदर्भ चर को छोड़ देते हैं जो ऑपरेटर जानते हैं कि मायने रखते हैं (तापमान उतार-चढ़ाव, रीagent लॉट नंबर, सूक्ष्म प्रोटोकॉल विचलन)।
- क्रिया अंतर: कई एआई सिस्टम यह सिफारिश कर सकते हैं कि क्या करना है, लेकिन वे विश्वसनीय रूप से सिफारिशों को मान्य भौतिक चरणों में अनुवाद नहीं कर सकते हैं।
- प्रतिक्रिया अंतर: निष्पादन से संरचित, उच्च गुणवत्ता वाली प्रतिक्रिया के बिना, मॉडल यह सीख नहीं सकते हैं कि वे कहां विफल होते हैं – और वैज्ञानिक यह नहीं जान सकते कि क्यों।
इन अंतराल को बंद करना नए न्यूरल नेटवर्क आर्किटेक्चर का आविष्कार करने के बारे में कम है और मशीनों के लिए प्रयोगशाला को स्पष्ट करने के लिए साधनों, इंटरफेस और डेटा अनुबंध बनाने के बारे में अधिक है, और एआई को मानवों के साथ काम करने की अनुमति देने के लिए।
डिजाइन द्वारा विश्वास: एआई जो कार्य कर सकता है के लिए सुरक्षा और शासन
अनुसंधान में एजेंटिक एआई न केवल सटीकता के बारे में परिचित चिंताओं को उठाता है। यह नए विफलता मोड की शुरुआत करता है क्योंकि यह कार्य कर सकता है। एक प्रयोगशाला में, क्रिया बर्बादी, नुकसान, या भ्रामक निष्कर्षों की संभावना को दर्शाती है, विशेष रूप से जब प्रयोग क्लिनिकल परिकल्पनाओं में खिलाते हैं।
एक उपयोगी मानसिकता यह है कि एआई-सक्षम लैब स्टैक को एक सामाजिक-तकनीकी प्रणाली के रूप में माना जाए जिसे आश्वासन की आवश्यकता है। कई मौजूदा ढांचे मदद करते हैं, लेकिन उन्हें प्रयोगशाला वास्तविकता में अनुवादित किया जाना चाहिए:
- जोखिम प्रबंधन एक निरंतर अभ्यास के रूप में: एनआईएसटी का एआई जोखिम प्रबंधन ढांचा (एआई आरएमएफ 1.0) जोखिम को मैप करने, मापने और प्रबंधित करने के लिए एक व्यावहारिक शब्दावली प्रदान करता है। एआई जोखिम के पूरे जीवन चक्र में।
- चिकित्सा संबंधित एआई के लिए नियामक संरेखण: एफडीए का एआई / एमएल सॉफ्टवेयर एक चिकित्सा उपकरण (एसएएमडी) के रूप में काम, जिसमें इसकी एक्शन प्लान और संबंधित दिशानिर्देश शामिल हैं, “अच्छी प्रथा” का एक ठोस दृश्य प्रदान करता है जब एआई रोगी देखभाल को प्रभावित करता है।
जीन संपादन और अन्य उच्च परिणामी डोमेन के लिए, शासन पहले से ही एक वैश्विक बातचीत है। मानव जीनोम संपादन पर अनुशंसाओं पर चर्चा की जा रही है, जिसमें उपयुक्त पर्यवेक्षण तंत्र और जिम्मेदार शासन पर जोर दिया जा रहा है, जैसे कि अमेरिकन सोसाइटी फॉर जीन एंड सेल थेरेपी, या एएसजीसीटी द्वारा आगे रखा गया है। लैबओएस जैसी प्रणालियों को इस तरह से डिज़ाइन किया जाना चाहिए कि अनुपालन को आसान बनाया जाए, न कि कठिन।
चेकलिस्ट: वैज्ञानिक खोज के लिए सुरक्षित एआई सह-वैज्ञानिकों के लिए नियंत्रण
हमारे दृष्टिकोण से, एक सुरक्षा-सचेत लैब ओएस को निम्नलिखित डिज़ाइनों को लागू करना चाहिए:
- प्रोवेनेंस डिफ़ॉल्ट रूप से: प्रत्येक डेटासेट, प्रोटोकॉल संस्करण, और मॉडल आउटपुट को इनपुट और टाइमस्टैम्प से ट्रेसेबल होना चाहिए।
- बाउंडेड स्वायत्तता: प्रणाली के पास स्पष्ट अनुमतियां (क्या यह पुष्टि के बिना कर सकता है) और एस्केलेशन नियम (जब यह पूछना होगा) होनी चाहिए।
- मानव ओवरराइड और क्रमिक गिरावट: जब सेंसर या डेटा स्ट्रीम विफल होते हैं, या अनिश्चितता उच्च होती है, तो प्रणाली को एक सुरक्षित, सरल मोड में वापस आना चाहिए।
- निरंतर मान्यकरण: सिलिको पूर्वानुमानों को शारीरिक प्रयोगशाला मान्यकरण के साथ जोड़ा जाना चाहिए; शारीरिक प्रयोगशाला रन में क्यूसी गेट्स शामिल होनी चाहिए इससे पहले कि निष्कर्ष डाउनस्ट्रीम वापस डिजिटल दुनिया में एआई मॉडल / एजेंटों में प्रसारित हों।
- सुरक्षा और द्वि-उद्देश्य जागरूकता: लैब इंफ्रास्ट्रक्चर को छेड़छाड़ से बचाएं।
मानवों को हर जगह सशक्त बनाना: क्या एआई सह-वैज्ञानिक मैदान को समतल कर सकते हैं?
एआई-एक्सआर “सह-वैज्ञानिक” का एक सबसे प्रेरक वादा यह नहीं है कि यह शीर्ष संस्थानों के लिए गति है, बल्कि यह हर किसी के लिए पहुंच योग्य है। विचार करें कि वर्तमान में क्या छोटी प्रयोगशालाओं, स्टार्टअप्स, और दूरस्थ / ग्रामीण / क्षेत्रीय क्लीनिकों को सीमित करता है:
- विशेषज्ञता के लिए सीमित पहुंच, सोने के मानक प्रोटोकॉल और उपकरणों के लिए।
- प्रशिक्षण, गलतियों, और पुनर्काम की लागत अधिक है।
- टूलिंग खंडित: नोटबुक, स्प्रेडशीट, इंस्ट्रूमेंट लॉग, और विश्लेषण स्क्रिप्ट शायद ही कभी साफ-साफ जुड़ते हैं।
एक प्रणाली जो संदर्भ में निष्पादन (एक्सआर ग्लास के माध्यम से) को मार्गदर्शन कर सकती है, स्वचालित रूप से क्या हुआ था उसे कैप्चर कर सकती है, और पिछले रनों के आधार पर अगले सर्वोत्तम चरण का सुझाव दे सकती है, उन्नत परीक्षणों को अधिक पुनरुत्पादक बना सकती है जो साइटों में वितरित की जा सकती हैं। सिद्धांत रूप में, यह वितरित नैदानिक अनुसंधान का भी समर्थन कर सकता है जहां प्रोटोकॉल को लगातार निष्पादित किया जाना चाहिए, भले ही संसाधन भिन्न हों।
टाइमलाइन: कब हर वैज्ञानिक और चिकित्सक को एक सह-वैज्ञानिक मिलेगा?
संक्षेप में, हम कुछ उच्च-मूल्य, उच्च-आवृत्ति कार्यों (जैसे प्रयोगशाला में एक दवा का विश्वसनीय उत्पादन) के लिए करीब हैं और दूसरों (जैसे कि कैंसर या अल्जाइमर जैसी बड़ी समस्याओं का पूरी तरह से हल करने) के लिए अधिकांश डेमो से दूर हैं। एक वास्तविक रोडमैप इस प्रकार दिखता है:
- निकट अवधि (1 वर्ष के भीतर): कार्य प्रवाह कोपायलट जो प्रशासनिक भार को कम करते हैं: प्रोटोकॉल ड्राफ्टिंग, साहित्य संश्लेषण, विश्लेषण टेम्पलेट, और स्वचालित क्यूसी रिपोर्ट। सीमित कारक एकीकरण है, न कि मॉडल क्षमता।
- मध्य अवधि (1-2 वर्ष): प्रयोगशाला में सह-कार्यान्वयन प्रणाली: एक्सआर ग्लास मार्गदर्शन, स्वचालित प्रलेखन, और पुनरावृत्ति चरणों के लिए चयनात्मक रोबोटिक्स। विश्वास ऑडिट ट्रेल्स और तंग मानव-इन-द-लूप डिजाइन पर निर्भर करेगा।
- लंबी अवधि (3+ वर्ष): क्रॉस-डोमेन सह-शोधकर्ता जो खोज को अनुवाद से जोड़ते हैं: लैब डेटा को नैदानिक परिणामों से जोड़ना, सुरक्षा संकेतों की निगरानी करना, और परीक्षणों को डिजाइन करने में मदद करते हुए – नियामक और नैतिक अपेक्षाओं का पालन करते हुए।
कोड से इलाज तक: 1000x वैज्ञानिक खोज के लिए आगे का रास्ता
लैबओएस एक सरल प्रश्न का उत्तर देने का एक प्रयास है: क्या होगा अगर एक प्रयोग एक बातचीत के रूप में चलाया जा सकता है, जहां इरादा, निष्पादन, और साक्ष्य अंत से अंत तक जुड़े हुए हैं? यदि हम इन प्रणालियों को अच्छी तरह से बनाते हैं, तो वे जैव चिकित्सा और कई भौतिक विज्ञान अनुशासनों (जैसे सामग्री विज्ञान) को धीमा करने वाले अनुवाद अंतर को संबोधित करने में मदद कर सकते हैं। यदि हम उन्हें खराब तरीके से बनाते हैं, तो वे पुनरुत्पादकता को बढ़ाते हैं और नए सुरक्षा जोखिम पैदा करते हैं।
अगले कुछ वर्षों में सबसे महत्वपूर्ण कार्य आधारभूत होगा: मानकीकृत डेटा और डिवाइस इंटरफेस का निर्माण (जैसे आईओएस सभी प्रकार के ऐप्स चलाता है), एआई बेंचमार्क बनाना जिसमें निष्पादन और अनिश्चितता शामिल है (जैसे लैबओएस में लैबसुपरविजन बेंचमार्क), और वास्तविक दुनिया में तैनाती शुरू करना जो नवाचार को प्रोत्साहित करती है जबकि रोगियों और अनुसंधान की अखंडता की रक्षा करती है।
शोधकर्ताओं और चिकित्सकों के लिए, प्रश्न यह नहीं है कि क्या एआई प्रयोगशाला में प्रवेश करेगा। यह पहले से ही है। प्रश्न यह है कि क्या हम इसे विच्छिन्न उपकरणों के संग्रह के रूप में एकीकृत करेंगे या वास्तविक जैव चिकित्सा विज्ञान की वास्तविकता के लिए डिज़ाइन की गई एक विश्वसनीय, लेखा परीक्षित प्रणाली के रूप में।
सुझाई गई पढ़ाई और स्रोत
- पुनरुत्पादकता सर्वेक्षण (नेचर, 2016): https://www.nature.com/articles/533452a
- सीआरआईएसपीआर-जीपीटी पियर-रिव्यूअर्ड लेख (नेचर बायोमेडिकल इंजीनियरिंग): https://www.nature.com/articles/s41551-025-01463-z
- स्टैनफोर्ड मेडिसिन न्यूज़ ऑन सीआरआईएसपीआर-जीपीटी (2025): https://med.stanford.edu/news/all-news/2025/09/ai-crispr-gene-therapy.html
- लैबओएस प्रीप्रिंट (arXiv): https://arxiv.org/abs/2510.14861
- लैबओएस और लैबसुपरविजन बेंचमार्क वेबसाइट: https://ai4lab.stanford.edu
- एनआईएसटी एआई जोखिम प्रबंधन ढांचा (एआई आरएमएफ 1.0): https://nvlpubs.nist.gov/nistpubs/ai/NIST.AI.100-1.pdf
- एफडीए का एआई / एमएल सॉफ्टवेयर एक चिकित्सा उपकरण के रूप में अवलोकन: https://www.fda.gov/medical-devices/software-medical-device-samd/artificial-intelligence-software-medical-device
- फेयर डेटा सिद्धांत (वैज्ञानिक डेटा, 2016): https://doi.org/10.1038/sdata.2016.18
- Unite.AI छोटे अणु ड्रग डिस्कवरी में बोतलें: https://www.unite.ai/how-ai-is-breaking-down-the-bottlenecks-in-small-molecule-drug-discovery/
- Unite.AI रोबोटिक सर्जरी में एआई: https://www.unite.ai/how-ai-is-ushering-in-a-new-era-of-robotic-surgery/












