Artificial Intelligence
DeepMind gotowy przekształcić nauki biologiczne poprzez rozwiązanie problemu zwijania białek
Dział sztucznej inteligencji Google, DeepMind, niedawno to zrobił dokonał znacznego postępu w kierunku rozwiązania jednego z najstarszych wyzwań biologii, obliczanie kształtu białka na podstawie sekwencji aminokwasów. Według Nature przełom może zmienić dziedziny biologii i chemii, umożliwiając naukowcom określenie funkcji wielu białek, które są obecnie tajemnicze.
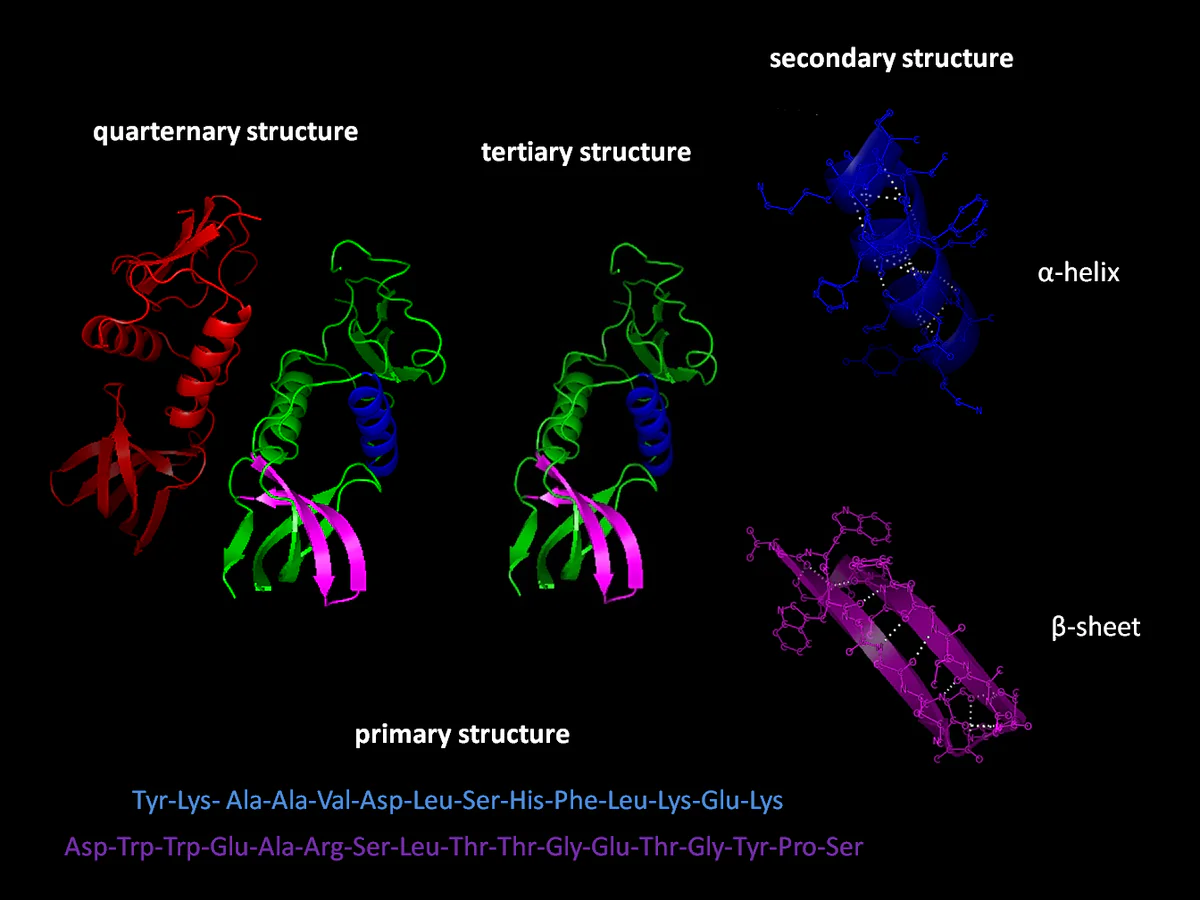
Kształt białka określa jego funkcję, a większość funkcji biologicznych zależy od białek. "Fałdowanie białek" to nazwa nadana procesowi przekształcającemu łańcuchy aminokwasów w trójwymiarowe struktury wymagane przez protiony do wykonywania swoich funkcji. Jeśli naukowcom uda się określić związek między sekwencjami aminokwasów a kształtem wytwarzanych przez nie białek, będą mogli określić, które białka wpływają na różne procesy biologiczne.
Naukowcy stawiają hipotezę, że w ludzkim proteomie znajduje się co najmniej 80,000 XNUMX białek, ale tylko niewielka część tych białek ma znaną strukturę. Tradycyjna metoda określania kształtu białka może wymagać lat eksperymentów laboratoryjnych, nawet przy wykorzystaniu mocy algorytmów i modeli informatycznych. Prace wykonane przez DeepMind mogą radykalnie przyspieszyć proces odkrywania struktur białek, wiarygodnie określając strukturę białek w ułamku normalnego czasu.
Naukowcy z DeepMind przeszkolili swoje algorytmy na bazie danych składającej się z około 170,0000 100 sekwencji białek i kształtów odpowiadających tym sekwencjom. Algorytmy opracowane przez badaczy zostały przeszkolone na od 200 do XNUMX procesorów graficznych, a proces uczenia trwał kilka tygodni. Model opracowany przez badaczy nazwano „AlphaFold”.
AlphaFold działa poprzez „algorytm napięcia”, zaczynając od łączenia ze sobą małych kawałków białka, a następnie zwiększając skalę, aby połączyć coraz większe sekcje. Najpierw połączono ze sobą małe klastry aminokwasów, a następnie algorytm szukał sposobów na połączenie tych klastrów.
Naukowcy z projektu AlphaFold początkowo próbowali wykorzystać konwencjonalne algorytmy głębokiego uczenia się na danych genetycznych i strukturalnych, aby przewidzieć związek między aminokwasami i białkami. Następnie AlphaFold stworzył modele konsensusowe dotyczące stylu białek. Kiedy okazało się, że technika ta ma zbyt wiele ograniczeń, badacze wypróbowali nową strategię. Zespół badawczy AlphaFold stworzył modele wyszkolone w zakresie większej liczby funkcji i tym razem dysponował przewidywaniami zwrotu modelu dla ostatecznej struktury sekwencji białkowych.
Zespół inżynierów przetestował AlphaFold, biorąc go do konkursu, w którym algorytmy komputerowe rywalizują o ocenę struktury białka na podstawie sekwencji aminokwasów. Konkurs nosił nazwę „Krytyczna ocena przewidywania struktury białka”, w skrócie CASP. Uczestnicy konkursu otrzymują do dyspozycji 100 sekwencji aminokwasów, a ich modele muszą opracować strukturę białek. AlphaFold nie tylko pobił inne modele komputerowe pod względem dokładności, ale także działał porównywalnie z tradycyjnymi technikami modelowania laboratoryjnymi. Końcowa mediana wyniku AlphaFold wyniosła około 92 na 100, a laboratoryjnym metodom eksperymentalnym przyznano wynik 90. Mediana wyniku AlphaFold w przypadku najtrudniejszych białek spadła do 87 procent.
Według dyrektora naczelnego i współzałożyciela DeepMind, Demisa Hassabisafirma planuje już udostępnienie badaczom AlphaFold, a naukowcy z Instytutu Biologii Rozwoju im. Maxa Plancka wykorzystali już ten model do odkrycia struktur białkowych, nad którymi pracowali przez ponad dekadę.
Janet Thornton, emerytowana dyrektor Europejskiego Instytutu Bioinformatyki, był cytowany przez ScienceMag jako stwierdzenie, że osiągnięcia DeepMind „zmienią przyszłość biologii strukturalnej i badań nad białkami”. Tymczasem biolog z Uniwersytetu Maryland w Shady Grove mówi John Moult że nigdy nie sądził, że problem zwijania się białek nigdy nie zostanie rozwiązany w tym życiu.
Chociaż jest mało prawdopodobne, że AlphaFold całkowicie zastąpi tradycyjne, eksperymentalne metody odkrywania struktur białkowych, może radykalnie zwiększyć szybkość odkrywania struktur białkowych. Do określenia struktury białka badacze mogą potrzebować mniej wysokiej jakości danych eksperymentalnych, a badacze mają już dostęp do dużej ilości danych genomicznych, które można przełożyć na struktury przy użyciu rozwiązań AlphaFold.














