Helse
AI sin rolle i medisinske bilder for tidligere anomaliopptak
Hypeen rundt AI er fremdeles dominerende i helsevesenet, men er særlig sterk i radiologi. Hvis du husker de tidlige dagene med datamaskinbasert design (CAD), er det ganske imponerende å se hvor langt teknologien har kommet. En innfødt av ChatGPT ville kanskje hevde at mye arbeid må gjøres før AI kan nå sitt fulle potensiale i dette feltet. Begge synspunkter er korrekte. Denne artikkelen vil undersøke hvorfor det er så vanskelig for AI å oppdage ting, hvordan dens rolle endrer seg, og hva trendene er å se i 2025 og utover.
Å finne en nål i en høystak: Oppdaging er vanskelig.
Å oppdage sykdom tidlig er vanskelig fordi sykdommer ofte starter med ganske sublime avvik fra normalt utseende i radiologiske bilde-data. Fordi det er mye helt normal, naturlig variasjon mellom individer, er det svært vanskelig å bestemme hvilke mindre endringer som faktisk er unormale. For eksempel begynner lungeknuter å være svært små; diffuse lunge-sykdommer begynner med lett overseende vevendringer.
Dette er der Machine Learning (ML) spiller en viktig rolle. Den kan lære å gjenkjenne de spesifikke endringene som ikke er normale, men heller er assosiert med sykdom og skille dem fra normal variasjon. Denne normale variasjonen kan ha forskjellige kilder: individuell anatomi, tekniske forskjeller i bilde-erhverelsesutstyr, eller selv tidsmessige endringer i vevets utseende som er fullstendig normale. Vi må trene ML-modeller med store mengder data så de kan danne representasjoner av denne variasjonen og identifisere de endringene som peker på sykdom.
Kan AI hjelpe oss med å oppdage anomali tidligere?
AI kan hjelpe på flere måter. Først kan den gjenkjenne spesifikke mønster som er assosiert med sykdom, som kreft, interstitielle lunge-sykdommer eller hjerte- og karsykdommer i bilde-data. Ved å trene på så divers data som mulig, kan AI robust oppdage funn som er viktige for den første diagnosen. Og ved å parsere hele bildevolumer, kan den støtte radiologer ved å høydeppe mistenkelige områder, og dermed øke legers sensitivitet.
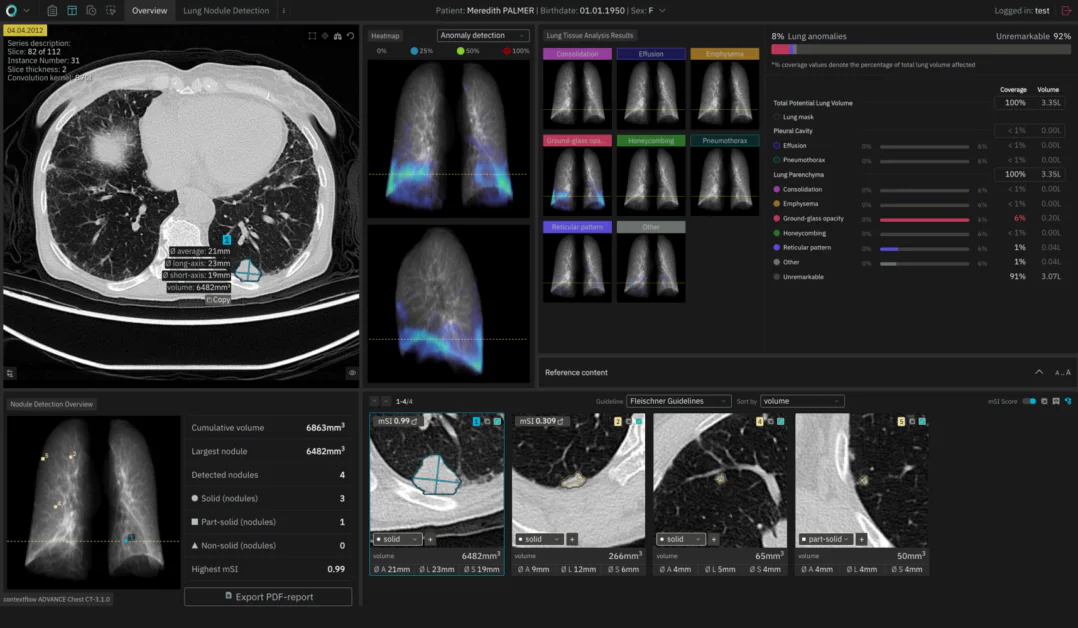
For det andre kan AI bruke bilde-egenskaper utover det mennesker lett kan observere og rapportere. I lungekreft-oppdaging, vurderer radiologer først størrelsen, formen og kategorien til en knute for å bestemme neste handling i pasientbehandling. AI kan analysere tredimensjonale teksturer og fine-kornede karakteristika av en knutes overflate for å mer pålitelig bestemme om den bærer en høy eller lav risiko for malignitet. Dette har direkte konsekvenser i håndtering av enkeltpasienter, som om personen skal sendes for biopsi eller lengden og hyppigheten av oppfølgingsintervaller.
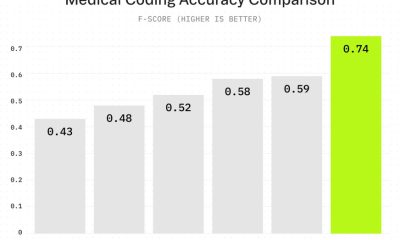
I en studie av Adams et al. (JACR), ble det vist at paring av retningslinje-basert håndtering av tilfeldige knuter i bryst-CT med ML-basert analyse kunne signifikant redusere falske positiver. Dette oversettes til både et reduert antall unødvendige biopsier (for tilfellene hvor AI sier knuten er godartet) og raskere tid til behandling (for tilfellene hvor AI sier knuten er ondartet). Her er det viktig å understreke – AI er ikke tilhenger av å eliminere retningslinjer. I stedet utfordres vi til å komplementere de nødvendige retningslinjene med AI-resultater. I dette tilfellet, hvis ML-poengene motsier retningslinjen med høy sikkerhet, gå med ML-poengene; ellers følg retningslinjene. Vi vil se flere applikasjoner som denne i fremtiden.
Tredje, kan AI hjelpe til å kvantifisere endring over tid hos pasienter, som igjen er avgjørende for riktig oppfølging. Gjeldende algoritmer i området ML og medisinsk bilde-analyse kan justere flere bilder fra samme pasient – vi kaller dette “registrering” – så vi kan se på samme posisjon på forskjellige tidspunkter. I tilfelle lungekreft, tillater tilføyning av sporingsalgoritmer oss å presentere hele historien til hver knute i en lunge til radiologer når de åpner en sak. I stedet for å måtte se opp tidligere skanninger og navigere til riktig posisjon for noen eksempler på knuter, ser de alt på en gang. Dette bør ikke bare frigjøre tid, men også gjøre for en mer behagelig arbeidserfaring for legene.
Radiologi vil utvikle seg på grunn av AI. Spørsmålet er, hvordan?
Det er flere retninger hvor AI utvikler seg raskt. Den åpenbare er at vi samler inn mer divers og representativ data for å bygge robuste modeller som fungerer godt i kliniske settinger. Dette inkluderer ikke bare data fra forskjellige typer skannere, men også data relatert til komorbiditet som gjør det vanskeligere å oppdage kreft.
Foruten data, er det en kontinuerlig fremgang i utvikling av nye ML-metoder for å forbedre nøyaktigheten. For eksempel er ett større forskningsområde å se på hvordan man kan skille biologisk variasjon fra forskjeller i bilde-erhverelsesutstyr; et annet område er å se på hvordan man kan overføre ML-modeller til nye domener. Multi-modalitet og prediksjon representerer to spesielt spennende retninger som også antyder hvordan radiologi kan endre seg over de neste årene. I presisjonsmedisin er integrert diagnostikk en kritisk retning som retter seg mot å bruke data fra radiologi, laboratorie-medisin, patologi og andre diagnostiske områder for behandlingsbeslutninger. Hvis disse dataene brukes sammen, tilbyr de mye mer informasjon til å guide beslutninger enn noen enkelt parameter alene. Dette er allerede standard praksis, for eksempel i tumor-boards; ML vil bare komme inn i diskusjonen fremover. Dette stiller spørsmålet: hva skal ML-modellene gjøre med all denne integrerte data fra flere kilder? En ting vi kunne gjøre er å prøve å forutsi fremtidig sykdom så vel som enkeltpersoners respons på behandling. Sammen holder de mye makt som vi kan utnytte til å skape “hva-hvis”-forutsigelser som kan guide behandlingsbeslutninger.
Trender for 2025: Forming Effektivitet, Kvalitet og Refusjon
Det er flere faktorer som driver AI i klinisk praksis. To viktige aspekter er effektivitet og kvalitet.
Effektivitet
Ved å la radiologer konsentrere seg om det kritiske og utfordrende aspektet av deres arbeid – integrering av kompleks data – kan AI hjelpe til å øke effektiviteten. AI kan støtte dette ved å gi kritisk og relevant informasjon på punktet for omsorg – f.eks. kvantitative verdier – eller ved å automatisere noen oppgaver som oppdaging eller segmentering av en anomali. Dette har en interessant sideeffekt: det ikke bare muliggjør en raskere vurdering av endringer, men også bringer oppgaver som piksel-for-piksel-segmentering og volumetri av sykdomsmønster fra forskning til klinisk praksis. Manuell segmentering av store mønster er fullstendig urealistisk i mange omstendigheter, men automatisering gjør denne informasjonen tilgjengelig under rutine-omsorg.
Kvalitet
AI påvirker kvaliteten av arbeidet. Det vil si: å bli bedre til å diagnostisere, anbefale spesifik behandling, tidligere oppdage sykdom eller mer nøyaktig vurdere behandlingsrespons. Disse er fordeler for hver enkelt pasient. For øyeblikket vurderes forholdet mellom disse fordelene og kost-efektivitet på et systemnivå for å studere og sammenligne helseøkonomisk påvirkning av innføringen av AI i radiologi.
Refusjon
AI-tilpasning er ikke lenger bare om effektivitet; det blir anerkjent og belønnet for sine konkrete bidrag til pasientbehandling og kostebesparelse. Dets inklusjon i refusjonssystemer understreker denne skiftningen. Mens fordelene – som reduksjon av unødvendige prosedyrer og akselerasjon av behandling – kan synes enkle i etterkant, har reisen vært lang. Nå, med de første suksessfulle tilfellene som dukker opp, er AI sin transformative påvirkning tydelig. Ved å forbedre pasientresultater og optimere helseprosesser, former AI industrien, med spennende utviklinger på horisonten.
Forming fremtiden for medisinske bilder
Medisinske bilder gjennomgår fundamentale transformasjoner. Presisjonsmedisin, integrert diagnostikk og ny molekylær diagnostisk teknologi endrer måtene å fatte behandlingsbeslutninger i et stadig mer komplekst landskap av terapi-alternativer. AI er en katalysator for denne endringen, ettersom den muliggjør for legene å integrere flere karakteristika fanget av forskjellige modaliteter og kobler dem til behandlingsresponser.
Det vil fortsatt ta tid å tilpasse disse verktøyene i stor skala på grunn av tekniske utfordringer, integreringsproblemer og helseøkonomiske bekymringer. En ting vi alle kan gjøre for å akselerere prosessen er å være en informert pasient. Vi kan alle snakke med våre leger om hva AI de måtte ha testet eller bruke i praksis og hvordan disse verktøyene komplementerer deres profesjonelle erfaring og kunnskap. Markedet taler til etterspørsel; så hvis vi etterspør tidlig, nøyaktig oppdaging, vil AI komme.