Sundhedsvæsen
Hvordan computer vision forbedrer kræftforskning

Computer vision er kunstig intelligens, der giver algoritmer mulighed for at udtrække meningsfuld information fra videoer og billeder. Kræftforskere har udforsket effektive måder at bruge det til at undersøge billeder, mikroskopiske prøver, medicinske scanninger og mere. Nogle tilgange kan forkorte tidligere besværlige arbejdsprocesser, sådan at ressourcestærke hold kan opnå mål og forhøje patientens indvirkning.
Forbedring af viden om tumorvækst
Efter at have bekræftet tilstedeværelsen og typen af kræft i biopsier, kan patologer udføre genetisk sekventering på RNA-molekylerne i prøverne. Derefter kan de finde ud af, hvilke genetiske ændringer, der påvirker tumorvæksten. Denne information fremmer værdifuld forskning og personlige interventioner. Men nuværende metoders høj omkostning og lange processer efterlader nogle forskere, der er ivrige efter at finde alternative løsninger.
Et hold byggede et AI-værktøj der analyserer standard mikroskopi billeder af biopsier for at forudsige den genetiske aktivitet inden for tumorceller. De trænede deres innovation på over 7.500 prøver, der repræsenterer 16 kræfttyper og andre relevante datasæt, herunder billeder af sunde celler.
Disse forskere prioriterede brugervenlighed gennem let fortolkning, og de skabte deres AI-drevne program til at vise den genrelaterede information som et visuelt tumorbiopsikort. Denne beslutning giver brugerne mulighed for at identificere karakteristiske variationer i bestemte områder. Gruppen afhængigt også af en standard farvemåde til at visualisere kræftceller, og værktøjet identificerede den genetiske udtryk af mere end 15.000 gener inden for de farvede billeder.
Deres fund tydede på en korrelation på over 80% mellem den AI-forudsagte genetiske aktivitet og den faktiske adfærd. Modellen udførte generelt bedre, når prøvedatasættet indeholdt flere eksempler på en bestemt kræfttype.
Forskningsholdets eksperimenter viste også algoritmens potentiale for at tildele genetiske risikoskorer til patienter med brystkræft. Parter, der blev klassificeret som mere risikable, havde flere tilbagefald og kortere perioder mellem dem.
Mennesker har brugt AI til andre fascinerende medicinske fremskridt. En udvikling kan detektere COVID-19 med op til 99% nøjagtighed, hvilket viser en væsentlig offentlig sundhedsforbedring. Trods disse muligheders imponerende karakter skal fagfolk kun supplere deres arbejde med dem. At lade AI erstatte førsteærhvervet erfaring kan reducere positive patientresultater.
At finde de mest passende behandlinger
Personer, der gennemgår kræftrelaterede interventioner, beskriver stress og ubehagelige symptomer forbundet med potentielt underoptimal løsninger. Selvom mange individer tåler kvalme, hårtab og mere, bliver de mindre enige om at fortsætte, hvis tidlige tests ikke viser lovende resultater.
Alle har gavn af, at kræftspecialister identificerer de bedste patient-specifikke behandlinger hurtigere. Den typiske tilgang til at designe behandlingsplaner indebærer at studere CT- og MRI-scanninger med kun ét datapunkt per pixel, repræsenteret som skyggefarver. Nogle forskere bruger AI til at gøre fremskridt. Et værktøj kan undersøge op til 30.000 detaljer per pixel og analysere vævsprøver så små som 400 kvadratmikrometer — omtrent bredde på fem menneskehår.
Holdet brugte donerede prøver til at vurderere resultaterne. Når det blev anvendt til blærekkræfttilfælde, fandt AI-platformen en specialiseret cellegruppe, der skaber tertiære lymfoid strukturer. Nuverende viden tyder på, at disse forbedrer patienternes immunterapirespons. Derudover differentierede værktøjet mellem kræftceller og vævsmukosa i mavesækkræftprøver, hvilket hjælper brugerne med at mere præcist bestemme omfanget af deres spredning.
Disse forskere mener, at deres bestræbelser kunne vise læger, hvilke behandlinger der fungerer bedst for forskellige kræftformer. Hvis det er tilfældet, kan det også strømline relevant forskning ved at hjælpe dem med at udtrække mere værdifuld data fra almindelige diagnostiske billeder.
At forkorte lægemiddeludviklingstider
At gøre nye kræftbehandlinger kommercielt tilgængelige tager år, og udsigterne afhænger af succesfulde kliniske forsøg. Forskere i London skabte nyligt en AI-aktiveret tilgang til at studere, hvor godt lægemidler når deres mål. Fokus på de mest effektive muligheder kunne forbedre resultater, overbevisende regulatorer om at udvide produkttilgængelighed.
Gruppen brugte næsten 100.000 3D-mikroskopi billeder af melanomceller, og geometriske dybe læringsalgoritmer analyserede deres form. Tidligere bestræbelser fik kun to-dimensionelle data fra prøver på mikroskopeglas, men denne tilgang undersøger celler, som de fremtræder i kroppen. Derudover afslører den, hvordan de ændrer form på grund af bestemte behandlinger, og viser variationer på tværs af cellulære populationer.
Værktøjet var mere end 99% nøjagtigt i at detektere, hvordan bestemte lægemidler påvirkede cellerne. Det identificerede endda formændringer udløst af lægemidler, der målrettede forskellige proteiner.
Fordi AI afslørede biokemiske ændringer, mener forskerne, at deres innovation kunne fremhæve bestemte mål at betone med nye kræftmediciner. Derefter ville softwaren forkorte den prækliniske tidsramme fra tre år til tre måneder. Relateret til dette kunne det reducere forsøg med op til seks år, hurtigere finde patienterne, der er mest sandsynligt at have gavn af det, og pege på de almindelige bivirkninger.
At strømline kræftevalueringopgaver
AI har allerede forbedret kræftforskernes opgaver, men de fleste værktøjer kan kun håndtere enkelte dele af arbejdsprocessen. Det betyder, at medicinske specialister, der er interesseret i at integrere teknologien i deres arbejdsdag, skal lære at bruge flere produkter. Imidlertid ønsker nogle grupper at bygge flerformålsløsninger for at øge brugervenligheden.
Et hold byggede en model lignende ChatGPT. De brugte den til flere evaluative processer forbundet med 19 kræfttyper, visende dets fleksibilitet. Mere specifikt accelererede det evalueringopgaver for forbedret detection, prognose og behandlingsrespons. Udviklerne mener også, at deres innovation er den første til at forudsige og validere resultater på tværs af flere internationale patientgrupper.
AI-modellen læser digitale glas, der indeholder tumorprøver, analyserer de molekylære profiler og finder kræftceller. Den undersøgte også væv omkring væksten, hvilket indikerer, hvor godt patienter har reageret på standardbehandlinger eller viser forskerne, hvilke behandlinger, der er mindre effektive. Eksperimenter tydede på, at det var mere nøjagtigt end nuværende tilgængelige produkter. Derudover forbundt det bestemte tumor-karakteristika med forhøjet patientoverlevelse, hvilket potentielt kan låse op for nye forskningsområder.
Forskerne trænede modellen på 15 millioner ulabelde billeder opdelt i stykker afhængigt af interesseområder. En senere fase udsatte algoritmerne for 60.000 hele-glas-eksempler, der repræsenterer de 19 kræfttyper. Denne tilgang lærte AI at vurderere hele billeder for at få grundige resultater.
Derefter testede gruppen deres værktøj på 19.400 hele-glas-billeder fundet i 32 uafhængige datasæt. Fordi denne information kom fra 24 globale patientkohorter og hospitaler, giver det en præcis prøve på reelle livsbetingelser.
At forbedre værdien af biomedicinske mikroskopi billeder
Kræftforskere bruger biomedicinske mikroskopi billeder til at fremme deres arbejde, men eksisterende arbejdsprocesser tager dage til at undersøge disse data. Et hold udviklede en ny computer vision-teknik til at gøre disse væsentlige opgaver mere effektive. Den bruger maskinlæring til at analysere prøver og finde fælles karakteristika blandt kræfttumorer.
Værktøjet opnår resultater effektivt ved at undersøge flere områder af enkeltvækst og opfatte dem som en helhed. Andre produkter, der analyserer biomedicinske mikroskopi billeder, dividerer store tumorer i mindre stykker og behandler stykkerne som separate prøver. Imidlertid kan disse billeder indeholde op til 1 milliard pixels, så de er tidskrævende at studere.
Udviklerne forestiller sig, at klinikerne kunne lave næsten øjeblikkelige diagnoser fra tumor-billeder. Derefter ville disse fagfolk give informationen til kirurger, der udfører operationer for at fjerne kræftvæv, hvilket giver dem mulighed for at bruge de mest aktuelle indsigt.
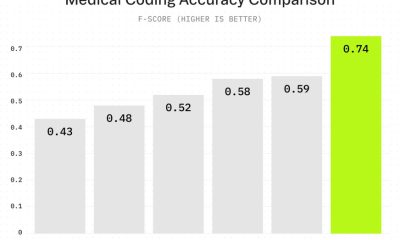
Tests, der sammenlignede dette værktøj med den bedst performende baseline billedanalyseteknik, viste, at det var næsten 4% bedre og opnåede næsten 88% nøjagtighed i visse tilfælde. Forskerne understregede også, at brugere kunne anvende det på enhver tumor-type og mikroskopi-metode, hvilket gør det bredt anvendeligt.
At fremme kræftforskning med computer vision
AI-drevet computer vision kan forbedre kræftforskernes output, maksimere deres videnskabelige og patientrelaterede resultater. Disse eksempler illustrerer det overvældende potentiale, men fagfolk, der er interesseret i at anvende teknologien, skal gøre det for at supplere erhvervet ekspertise og ikke behandle innovationer som fejlfri.