Sundhedsvæsen
AI’s rolle i medicinsk billedanalyse til tidligere afvigelsesdetektion
Hysteriet omkring AI er stadig til stede i sundhedssektoren, men er særligt stærk i radiologi. Hvis du husker de tidlige dage med computerstøttet design (CAD), er det ret imponerende, hvor langt teknologien er kommet. En indfødt af ChatGPT ville måske hævde, at der stadig er meget arbejde, der skal gøres, før AI kan nå sin fulde potentiale i dette felt. Begge synspunkter er korrekte. Denne artikel vil undersøge, hvorfor det er så svært for AI at detektere ting, hvordan dens rol ændrer sig, og hvilke tendenser, der skal følges i 2025 og derefter.
At finde en nål i en høstak: Detektion er svært.
At detektere sygdomme tidligt er svært, fordi sygdomme ofte begynder med ret subtile afvigelser fra normalt udseende i radiologiske billeddata. Fordi der er en masse helt normal, naturlig variation mellem individer, er det meget svært at bestemme, hvilke mindre ændringer, der virkelig er unormale. For eksempel begynder lungenknuder med at være meget små; diffuse lungenlidelser begynder med letoversete vævsændringer.
Det er her, Machine Learning (ML) spiller en vigtig rol. Den kan lære at genkende de specifikke ændringer, der ikke er normale, men snarere er forbundet med sygdom, og adskille dem fra normal variation. Denne normale variation kan have forskellige kilder: individuel anatomi, tekniske forskelle i billedindfangeselsesudstyr eller endda tidsmæssige ændringer i vævsudseende, der er helt normale. Vi skal træne ML-modeller med store mængder data, så de kan danne repræsentationer af denne variation og identificere de ændringer, der peger på sygdom.
Kan AI hjælpe os med at detektere afvigelser tidligere?
AI kan hjælpe på flere måder. Først kan den genkende specifikke mønstre, der er forbundet med sygdom, såsom kræft, interstitielle lungenlidelser eller hjertekarsygdom i billeddata. Ved at træne på så divers data som muligt kan AI robustt detektere fund, der er vigtige for den første diagnose. Og ved at parse hele billedvolumener kan den støtte radiologer ved at højligte mistænkelige områder, hvilket øger lægernes sensitivitet.
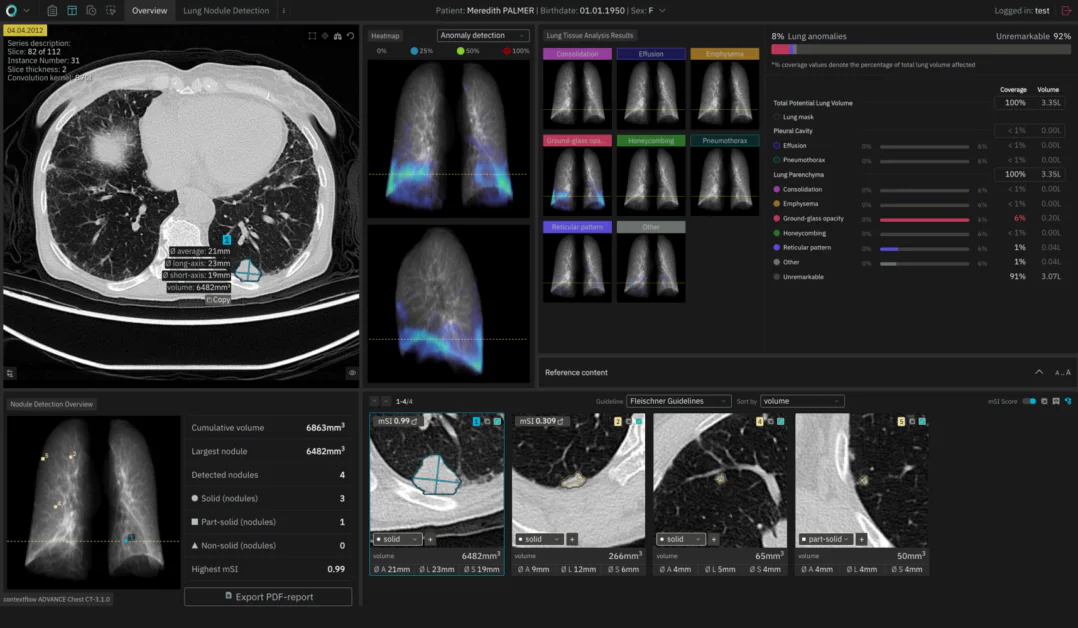
For det andet kan AI bruge billedfunktioner ud over det, som mennesker let kan observere og rapportere. I lungenkræftsdetektion vurderer radiologer først størrelsen, formen og kategorien af en knude for at beslutte om den næste handling i patientens behandling. AI kan analysere tre-dimensionelle teksturer og fine-grænseegenskaber af en knudes overflade for at mere pålideligt bestemme, om den medfører en høj eller lav risiko for malignitet. Dette har direkte konsekvenser for håndtering af enkeltpatienter, såsom om personen skal sendes til biopsi eller længden og hyppigheden af opfølgningsintervaller.
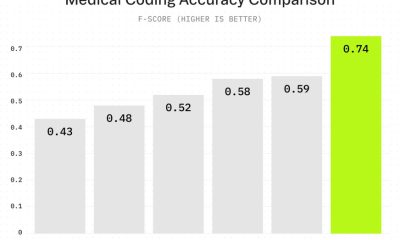
I en studie af Adams et al. (JACR) blev det vist, at paring af retningslinje-baseret håndtering af tilfældige knuder i bryst-CT med ML-baseret analyse kunne betydeligt reducere falske positiver. Dette oversætter sig til både et reduceret antal unødvendige biopsier (for tilfældene, hvor AI siger, at knuden er godartet) og hurtigere tid til behandling (for tilfældene, hvor AI siger, at knuden er ondartet). Her er det vigtigt at understrege – AI er ikke tilhænger af at eliminere retningslinjer. I stedet udfordres vi til at supplere de nødvendige retningslinjer med AI-resultater. I dette tilfælde, hvis ML-scoren modsiger retningslinjen med høj sikkerhed, så gå med ML-scoren; ellers fasthold retningslinjens instruktioner. Vi vil se mere af denne type af anvendelser i fremtiden.
For det tredje kan AI hjælpe med at kvantificere ændringer over tid hos patienter, hvilket igen er afgørende for ordentlig opfølgningsbehandling. Nuværende algoritmer i området ML og medicinsk billedanalyse kan aligne multiple billeder fra samme patient – vi kalder dette “registration” – så vi kan se på samme position på forskellige tidspunkter. I tilfældet af lungenkræft tillader tilføjelse af sporingalgoritmer os at præsentere hele historien om hver knude i en lunge for radiologerne, når de åbner en sag. I stedet for at skulle se på tidligere scanninger og navigere til den rigtige position for et par eksempler på knuder, ser de alt på én gang. Dette burde ikke kun frigøre tid, men også gøre det til en mere behagelig arbejdserfaring for lægerne.
Radiologi vil udvikle sig på grund af AI. Spørgsmålet er, hvordan?
Der er flere retninger, hvor AI udvikler sig hurtigt. Den åbenlyse er, at vi samler mere divers og repræsentativ data for at bygge robuste modeller, der fungerer godt i kliniske sammenhænge. Dette inkluderer ikke kun data fra forskellige typer scannere, men også data relateret til samtidige sygdomme, der gør det sværere at detektere kræft.
Foruden data er der en kontinuerlig fremgang i udviklingen af nye ML-metoder til at forbedre nøjagtigheden. For eksempel er et stort forskningsområde at se på, hvordan man kan skille biologisk variation fra forskelle i billedindfangeselse; et andet område er at se på, hvordan man kan overføre ML-modeller til nye domæner. Multi-modalitet og prædiktion repræsenterer to særligt spændende retninger, der også antyder, hvordan radiologi måske kan ændre sig over de næste få år. I præcisionsmedicin er integreret diagnostik en kritisk retning, der sigter mod at bruge data fra radiologi, laboratorie medicin, patologi og andre diagnostiske områder til behandlingsbeslutninger. Hvis disse data bruges sammen, tilbyder de langt mere information til at guide beslutninger end nogen enkelt parameter alene. Dette er allerede standardpraksis, for eksempel i tumorboard-møder; ML vil blot indgå i diskussionen fremover. Dette stiller spørgsmålet: Hvad skal ML-modellerne gøre med alle disse integrerede data fra multiple kilder? En ting, vi kunne gøre, er at prøve at forudsige fremtidig sygdom samt en enkelt persons respons på behandling. Sammen indeholder de en masse kraft, som vi kan udnytte til at skabe “hvad-hvis”-forudsigelser, der kan guide behandlingsbeslutninger.
Tendenser for 2025: Formning af effektivitet, kvalitet og refusion
Der er flere faktorer, der driver AI i klinisk praksis. To vigtige aspekter er effektivitet og kvalitet.
Effektivitet
Ved at låse radiologer til at koncentrere sig om det kritiske og udfordrende aspekt af deres arbejde – integration af komplekse data – kan AI hjælpe med at øge effektiviteten. AI kan støtte dette ved at give kritisk og relevant information på behandlingsstedet – f.eks. kvantitative værdier – eller ved at automatisere nogle opgaver, såsom detektion eller segmentering af en afvigelse. Dette har en interessant sideeffekt: det ikke kun gør vurderingen af ændringer hurtigere, men det bringer også opgaver som pixel-for-pixel-segmentering og volumetri af sygdomsmønstre fra forskning til klinisk praksis. Manuelt at segmentere store mønstre er fuldstændig ufeasible i mange situationer, men automation gør denne information tilgængelig under rutinebehandling.
Kvalitet
AI påvirker kvaliteten af arbejdet. Dette betyder: at blive bedre til diagnose, anbefaling af specifik behandling, tidligere detektion af sygdom eller mere præcis vurdering af behandlingsrespons. Disse er fordelene for hver enkelt patient. For øjeblikket vurderes forholdet mellem disse fordelene og omkostningseffektivitet på systemniveau for at studere og benchmarkere sundhedsøkonomiens impact af AI’s indførelse i radiologi.
Refusion
AI-adoptions er ikke længere kun om effektivitet; det bliver anerkendt og belønnet for sine konkrete bidrag til patientbehandling og omkostningsbesparelser. Dets inklusion i refusionsordninger understreger denne ændring. Mens fordelene – såsom reducering af unødvendige procedurer og accelerering af behandling – synes åbenlyse i retrospekt, har rejsen været lang. Nu, med de første succesfulde tilfælde, der dukker op, er AI’s transformative impact klar. Ved at forbedre patientresultater og optimere sundhedsprocesser former AI branchen, med spændende udviklinger på horisonten.
Formning af fremtidens medicinske billeder
Medicinsk billedanalyse undergår fundamentale forandringer. Præcisionsmedicin, integreret diagnostik og ny molekylær diagnostisk teknologi ændrer måden, behandlingsbeslutninger træffes på, i et stadig mere komplekst landskab af behandlingsmuligheder. AI er en katalysator for denne ændring, da den giver læger mulighed for at integrere mere karakteristika fanget af forskellige modaliteter og kobler dem til behandlingsresponser.
Det vil stadig tage tid at adoptere disse værktøjer i stor skala på grund af tekniske udfordringer, integrationsproblemer og sundhedsøkonomiske bekymringer. En ting, vi alle kan gøre for at accelerere processen, er at være en informeret patient. Vi kan alle tale med vores læger om, hvilke AI-værktøjer de måske har testet eller bruger i praksis, og hvordan disse værktøjer supplerer deres professionelle erfaring og viden. Markedet taler til efterspørgsel; så hvis vi efterspørger tidlig, præcis detektion, vil AI komme.