Artificial Intelligence
DeepMind、タンパク質のフォールディング問題を解決することで生物科学を変革する構え
GoogleのAI部門DeepMindは最近、 大きな進歩を遂げた 生物学における最も古い課題の XNUMX つの解決に向けて、アミノ酸配列からタンパク質の形状を計算します。 Nature によると、この画期的な進歩は生物学と化学の分野を変革する可能性があり、科学者は現在謎に包まれている多くのタンパク質の機能を決定できるようになります。
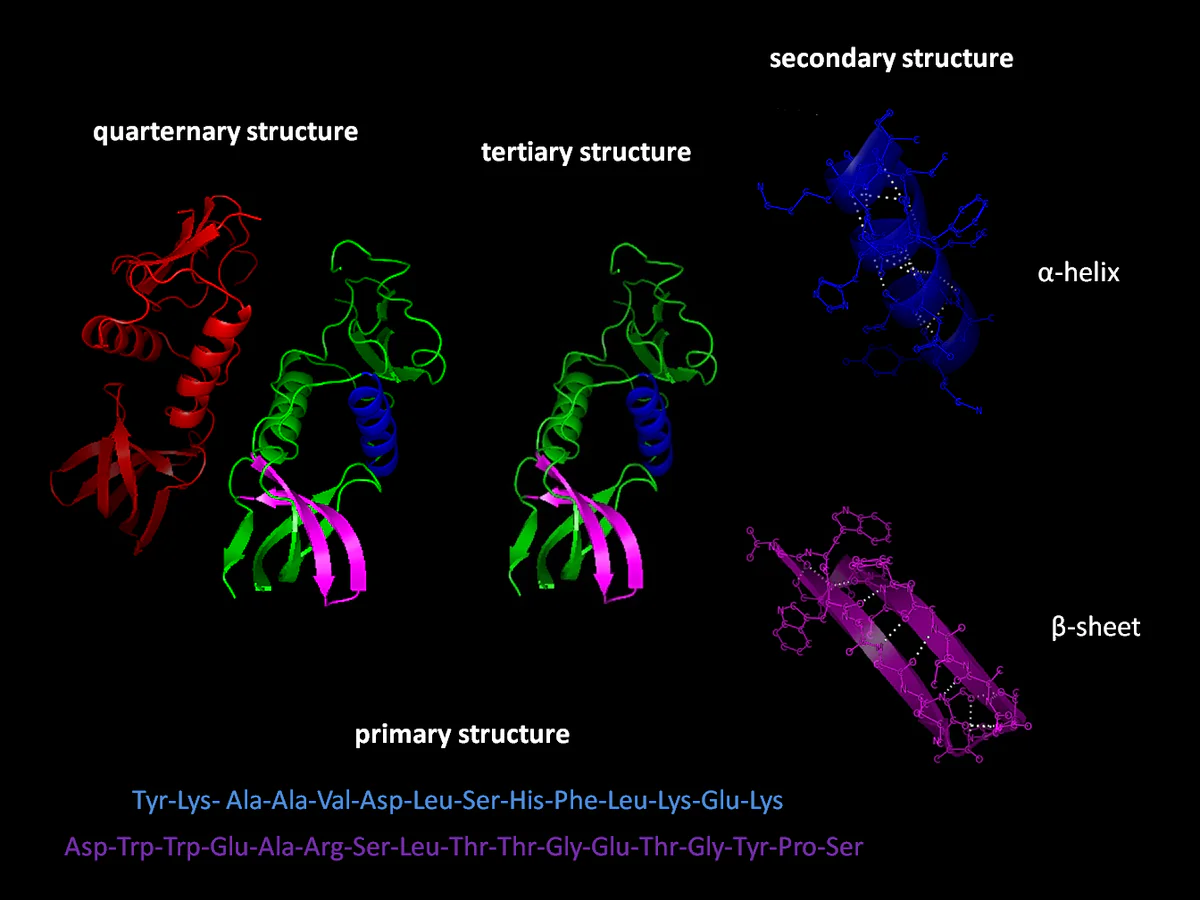
タンパク質の形状はその機能を定義し、ほとんどの生物学的機能はタンパク質に依存しています。 「タンパク質のフォールディング」 は、アミノ酸の鎖を、プロチオンがその機能を実行するために必要な三次元構造に変換するプロセスに与えられた名前です。 科学者がアミノ酸配列と生成するタンパク質の形状との関係を特定できれば、どのタンパク質がさまざまな生物学的プロセスに影響を与えるかを特定できるようになります。
科学者たちは、ヒトのプロテオーム内には少なくとも 80,000 個のタンパク質が存在するが、既知の構造を持っているタンパク質はそのうちのほんの一部だけであると仮説を立てています。 タンパク質の形状を決定する従来の方法では、コンピューターサイエンスのアルゴリズムやモデルの力を活用した場合でも、何年にもわたる実験室実験が必要になる場合があります。 DeepMind によって行われる作業により、タンパク質の構造を発見するプロセスが大幅にスピードアップされ、通常の時間の何分の一かでタンパク質の構造を確実に決定できます。
DeepMind の研究者は、約 170,0000 のタンパク質配列とそれらの配列に対応する形状で構成されるデータベースでアルゴリズムをトレーニングしました。 研究者らが開発したアルゴリズムは 100 ~ 200 個の GPU でトレーニングされ、トレーニング プロセスが完了するまでに数週間かかりました。 研究者らが開発したモデルは「AlphaFold」と名付けられた。
AlphaFold は「テンション アルゴリズム」を通じて動作します。最初はタンパク質の小さな断片を結合することから始まり、その後スケールアップしてより大きなセクションを結合します。 最初は小さなアミノ酸クラスターが互いにリンクされ、次にアルゴリズムはこれらのクラスターをリンクする方法を見つけようとしました。
AlphaFoldの研究者らは当初、アミノ酸とタンパク質の関係を予測するために、遺伝子データと構造データに対して従来の深層学習アルゴリズムを使用しようと試みた。 AlphaFold はその後、タンパク質のスタイルに関するコンセンサス モデルを作成しました。 この手法には制限が多すぎることが判明したため、研究者たちは新しい戦略を試みました。 AlphaFold 研究チームは、より多くの特徴についてトレーニングされたモデルを作成し、今回はそのモデルにタンパク質配列の最終構造の予測を返させました。
エンジニアリングチームは、コンピュータアルゴリズムがアミノ酸配列からタンパク質の構造を評価する競争にAlphaFoldを参加させ、AlphaFoldのストレステストを行った。 コンテストは「タンパク質構造予測の重要な評価」(CASP)でした。 コンテストの参加者には 100 個のアミノ酸配列が提供され、そのモデルはタンパク質の構造を解明しなければなりません。 AlphaFold は、精度の点で他のコンピューター モデルを上回っただけでなく、従来の研究室ベースのモデリング技術と同等のパフォーマンスを発揮しました。 AlphaFold の最終的な中央値スコアは 92 点中約 100 点で、ラボベースの実験方法には 90 点が割り当てられました。AlphaFold の中央値スコアは、最も困難なタンパク質では 87% に低下しました。
DeepMind の最高経営責任者兼共同創設者であるデミス・ハサビス氏によると、同社はすでに研究者にAlphaFoldへのアクセスを提供する計画を立てており、マックス・プランク発生生物学研究所の科学者たちはすでにこのモデルを利用してXNUMX年以上研究してきたタンパク質の構造を発見している。
欧州バイオインフォマティクス研究所名誉所長のジャネット・ソーントン氏は、 ScienceMag経由で引用されました DeepMind の成果は「構造生物学とタンパク質研究の未来を変えるだろう」と述べています。 一方、メリーランド大学の生物学者シェイディ・グローブ氏は、 ジョン・モルト 言う 彼は、タンパク質の折り畳みの問題がこの生涯で決して解決されないとは思ってもいなかったと述べた。
AlphaFold がタンパク質構造を発見する従来の実験的方法を完全に置き換える可能性は非常に低いですが、タンパク質構造の発見速度が劇的に向上する可能性があります。 研究者は、タンパク質の構造を決定するためにそれほど高品質の実験データを必要としない可能性がありますが、研究者はすでに、AlphaFold のソリューションを使用して構造に変換できる大量のゲノムデータにアクセスできます。














