Umjetna inteligencija
DeepMind spreman transformirati biološke znanosti rješavanjem problema savijanja proteina
Googleov AI odjel DeepMind nedavno je ostvario značajan napredak prema rješavanju jednog od najstarijih izazova u biologiji, izračunavanje oblika proteina iz niza aminokiselina. Prema Natureu, ovo otkriće ima potencijal transformirati polja biologije i kemije, omogućujući znanstvenicima da odrede funkciju mnogih proteina koji su trenutno misteriozni.
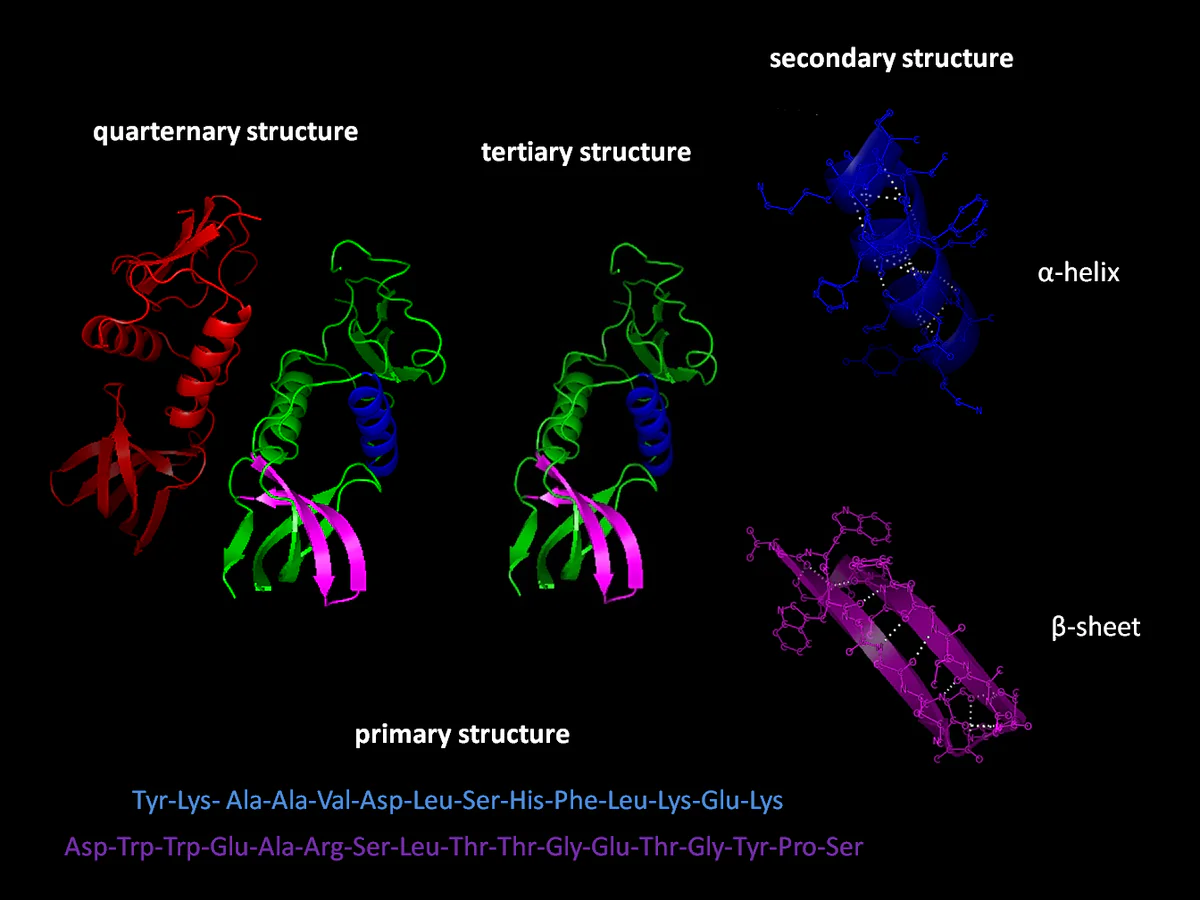
Oblik proteina definira njegovu funkciju, a većina bioloških funkcija ovisi o proteinima. “Savijanje proteina” je naziv dan procesu koji pretvara lance aminokiselina u trodimenzionalne strukture potrebne protionima za obavljanje njihovih funkcija. Ako znanstvenici mogu odrediti odnos između sekvenci aminokiselina i oblika proteina koje one stvaraju, mogu odrediti koji proteini utječu na različite biološke procese.
Znanstvenici pretpostavljaju da postoji najmanje 80,000 XNUMX proteina unutar ljudskog proteoma, ali samo mali dio tih proteina ima poznate strukture. Za tradicionalnu metodu određivanja oblika proteina mogu biti potrebne godine laboratorijskih eksperimenata, čak i korištenje snage računalnih znanstvenih algoritama i modela. Rad koji je obavio DeepMind može dramatično ubrzati proces otkrivanja proteinskih struktura, pouzdano određujući strukturu proteina u djeliću uobičajenog vremena.
Istraživači u DeepMindu trenirali su svoje algoritme na bazi podataka koja se sastoji od približno 170,0000 proteinskih sekvenci i oblika koji odgovaraju tim sekvencama. Algoritmi koje su razvili istraživači trenirani su na između 100 do 200 GPU-ova, a proces obuke trajao je nekoliko tjedana. Model koji su razvili istraživači nazvan je "AlphaFold".
AlphaFold radi kroz "algoritam napetosti", počevši spajanjem malih dijelova proteina zajedno, a zatim povećavajući kako bi povezao sve veće i veće dijelove. Mali klasteri aminokiselina prvo su bili međusobno povezani, a zatim je algoritam tražio načine za povezivanje tih klastera.
Istraživači AlphaFolda u početku su pokušali koristiti konvencionalne algoritme dubokog učenja na genetskim i strukturnim podacima kako bi predvidjeli odnos između aminokiselina i proteina. AlphaFold je zatim stvorio konsenzusne modele za stil proteina. Kad se pokazalo da ova tehnika ima previše ograničenja, istraživači su isprobali novu strategiju. Istraživački tim AlphaFolda stvorio je modele obučene na više značajki, a ovaj put su imali povratna predviđanja modela za konačnu strukturu proteinskih sekvenci.
Inženjerski tim testirao je AlphaFold na stres tako što ga je prijavio na natjecanje u kojem se računalni algoritmi natječu u procjeni strukture proteina iz sekvenci aminokiselina. Natjecanje je bilo “Kritička procjena predviđanja strukture proteina” ili CASP. Sudionici natjecanja dobivaju 100 sekvenci aminokiselina i njihovi modeli moraju razraditi strukturu proteina. Ne samo da je AlphaFold nadmašio ostale računalne modele u pogledu točnosti, nego je također imao performanse usporedive s tradicionalnim, laboratorijskim tehnikama modeliranja. AlphaFoldov konačni srednji rezultat bio je otprilike 92 od 100, s laboratorijskim eksperimentalnim metodama dodijeljenim rezultatom od 90. AlphaFoldov srednji rezultat pao je na 87 posto na najtežim proteinima.
Prema riječima izvršnog direktora i suosnivača DeepMinda Demisa Hassabisa, tvrtka već planira dati istraživačima pristup AlphaFoldu, a znanstvenici s Instituta Max Planck za razvojnu biologiju već koriste model za otkrivanje proteinskih struktura na kojima su radili više od desetljeća.
Janet Thornton, ravnateljica emeritus Europskog bioinformatičkog instituta, citirao je ScienceMag rekavši da će DeepMindova postignuća “promijeniti budućnost strukturne biologije i istraživanja proteina”. U međuvremenu, biolog sa Sveučilišta Maryland, Shady Grove, John Moult kaže da nikada nije mislio da problem savijanja proteina nikada neće biti riješen u ovom životu.
Iako je malo vjerojatno da će AlphaFold u potpunosti zamijeniti tradicionalne, eksperimentalne metode otkrivanja proteinskih struktura, mogao bi dramatično povećati brzinu otkrivanja proteinskih struktura. Istraživačima će možda trebati manje visokokvalitetnih eksperimentalnih podataka za određivanje strukture proteina, a istraživači već imaju pristup velikoj količini genomskih podataka koji se mogu prevesti u strukture korištenjem AlphaFoldovih rješenja.














